题目内容
7.某溶液含有K+、Fe3+、SO$\stackrel{2-}{4}$、OH-、I-中的几种.取样,滴加KSCN溶液后显红色.为确定该溶液的组成,还需检验的离子是( )| A. | K+ | B. | I- | C. | SO$\stackrel{2-}{4}$ | D. | CO$\stackrel{2-}{3}$ |
分析 滴加KSCN溶液后显血红色证明溶液中含有铁离子,铁离子和碳酸根离子、碘离子之间均能发生反应,溶液是电中性的.
解答 解:取样,滴加KSCN溶液后显血红色,证明溶液中含有铁离子,铁离子具有氧化性,可以和碘离子之间发生氧化还原反应,与氢氧根发生复分解,生成难溶的氢氧化铁,所以OH-、I-一定不能共存,无需检验,但是溶液中性的条件下决定溶液中必须含有阴离子,所以一定含有硫酸根离子,即硫酸根离子无需检验,而钾离子是否存在需要检验.
故选A.
点评 本题考查学生离子共存的有关知识,注意知识的归纳和整理是解题关键,难度不大.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
2.将10g铁碳合金放入O2中高温灼烧,反应后的气体通入到过量石灰水中得沉淀1.4g.则此铁碳合金是( )
| A. | 生铁 | B. | 高碳钢 | C. | 中碳钢 | D. | 低碳钢 |
18.设NA 为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 88.0g 干冰中含有的电子数为8.0NA | |
| B. | 常温下,11.2L乙烯在氧气中完全燃烧转移的电子数为6.0NA | |
| C. | 常温下1.0L0.1 mol•L-1NH4Cl 溶液中,NH4+和H+总数大于0.1NA | |
| D. | 1.2g金刚石中含有的碳碳键数为0.4NA |
15.在一定温度下,将nmolPCl5通入定容的密闭容器中,达平衡,反应为:PCl5(g)?PCl3(g)+Cl2(g),测得压强为P1,若再向容器中通入nmolPCl5,又达平衡后,压强为P2,则下列关系式正确的是( )
| A. | P1=2P2 | B. | 2P1=P2 | C. | P1<P2<2P1 | D. | 2P1<P2 |
2.以石墨电极电解200mL CuSO4溶液,电解过程中电子转移物质的量n(e-)与产生气体总体积V(g)(标准状况)的关系如图所示.下列说法中(忽略溶液体积变化)正确的是( )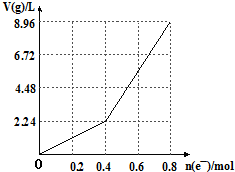

| A. | 电解前CuSO4溶液的物质的量浓度为2mol/L | |
| B. | 电解后所得溶液中c(H+)═2mol/L | |
| C. | 当n(e-)=0.6mol时,V(H2):V(O2)=3:2 | |
| D. | 向电解后的溶液中加入16gCuO,则溶液可恢复为电解前的浓度 |
12.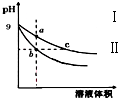 常温下,相同pH的氢氧化钠和醋酸钠溶液加水稀释,平衡时pH随溶液体积变化的曲线如图所示,则下列叙述正确的是( )
常温下,相同pH的氢氧化钠和醋酸钠溶液加水稀释,平衡时pH随溶液体积变化的曲线如图所示,则下列叙述正确的是( )
 常温下,相同pH的氢氧化钠和醋酸钠溶液加水稀释,平衡时pH随溶液体积变化的曲线如图所示,则下列叙述正确的是( )
常温下,相同pH的氢氧化钠和醋酸钠溶液加水稀释,平衡时pH随溶液体积变化的曲线如图所示,则下列叙述正确的是( )| A. | b、c两点溶液的导电能力相同 | |
| B. | a、b、c三点溶液中水的电离程度a>c>b | |
| C. | c点溶液中c (H+)=c (OH-)+c (CH3COOH) | |
| D. | 用等浓度的盐酸分别与等体积的b、c处溶液恰好完全反应,消耗盐酸体积 Vb=Vc |