题目内容
三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O═2NO+HNO3+9HF,下列有关该反应的说法正确的是( )
| A、NF3是氧化剂,H2O是还原剂 |
| B、还原剂和氧化剂的物质的量之比为2:1 |
| C、若生成0.2mol HNO3,则转移0.4mol电子 |
| D、按照树状分类法的分类原则,NF3属于盐 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:3NF3+5H2O=2NO+HNO3+9HF反应中,只有N元素的化合价发生变化,NF3既是氧化剂又是还原剂,从化合价的变化的角度分析氧化还原反应.
解答:
解:A.只有N元素的化合价发生变化,NF3既是氧化剂又是还原剂,故A错误;
B.NF3生成NO,被还原,NF3生成HNO3,被氧化,还原剂与氧化剂的物质的量之比为1:2,故B错误;
C.生成0.2molHNO3,转移的电子的物质的量为0.2mol×(5-3)=0.4mol,故C正确;
D.照树状分类法的分类原则,NF3属于共价化合物,不属于盐,故D错误;
故选C.
B.NF3生成NO,被还原,NF3生成HNO3,被氧化,还原剂与氧化剂的物质的量之比为1:2,故B错误;
C.生成0.2molHNO3,转移的电子的物质的量为0.2mol×(5-3)=0.4mol,故C正确;
D.照树状分类法的分类原则,NF3属于共价化合物,不属于盐,故D错误;
故选C.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素化合价的升降为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,注意从化合价的角度分析,题目难度不大.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
除去KNO3溶液中的少量Ca(NO3)2杂质,可以使用的方法为( )
| A、加入过量的Na2CO3溶液,过滤除去沉淀,所得溶液中补加适量稀HNO3 |
| B、加入过量的KCl溶液,过滤除去沉淀,所得溶液中补加适量稀HNO3 |
| C、加入过量的K2CO3溶液,过滤除去沉淀,所得溶液中补加适量稀HNO3 |
| D、加入过量的NaCl溶液,过滤除去沉淀,所得溶液中补加适量稀HNO3 |
下列判断不合理的是( )
| A、能电离出H+的物质一定是酸 |
| B、焰色反应是物理变化 |
| C、碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物 |
| D、蔗糖、碳酸钡和水分别属于非电解质、强电解质和弱电解质 |
设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A、200mL 1mol/L的NaCl溶液中阴阳离子总数为0.2NA |
| B、标准状况下,11.2L乙醇中的分子数为0.5NA |
| C、58.5gNaCl完全溶于2L水中,得到NaCl溶液的物质的量浓度为0.5mol/L |
| D、1mol金属Na与足量的O2反应生成Na2O和Na2O2混合物,Na失去的电子数为NA |
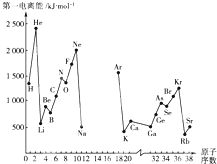 根据信息回答列问题:
根据信息回答列问题: