题目内容
A、B、C3种元素为短周期元素.A元素的阴离子不能被任何氧化剂氧化,则A离子为________离子.1 mol B单质能从盐酸中置换出3 g氢气,此时B转变为与Ne原子具有相同电子层结构的离子,则B元素是________;B的最高价氧化物的相应水化物的化学式为________.C元素有三个电子层,且最外电子层上的电子比L电子层少2个,则C元素是________;C与Na反应后生成化合物的化学键是________.
答案:
解析:
解析:
|
答案:F- Al Al(OH)3 S 离子键 思路解析:A元素的阴离子不能被任何氧化剂氧化,说明A元素的原子是最活泼的非金属F,则A离子为F-;1 mol B单质能从盐酸中置换出3 g氢气,即置换出1.5 mol氢气,B为三价金属,而反应后B转变为与Ne原子具有相同电子层结构的离子,则B元素是Al;B的最高价氧化物的相应水化物的化学式为Al(OH)3;C元素有3个电子层,且最外电子层比L电子层少2个电子,则C元素是S;C与Na反应生成Na2S,化学键是离子键. |

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
 (已折合成标准状况),取17.92gA完全燃烧,生成的气体通过浓
(已折合成标准状况),取17.92gA完全燃烧,生成的气体通过浓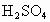 ,浓
,浓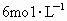 盐酸混,合加热可以完全水解,1molA水解成1molB和1molC.已知A、B、C3种物质均含有1个羟基,B物质仅由C、H、O
3种元素组成.其物质的量之比是7∶6∶2,C的俗名为甘氨酸,试写出化合物A的结构简式.
盐酸混,合加热可以完全水解,1molA水解成1molB和1molC.已知A、B、C3种物质均含有1个羟基,B物质仅由C、H、O
3种元素组成.其物质的量之比是7∶6∶2,C的俗名为甘氨酸,试写出化合物A的结构简式.