题目内容
8.在n(NO3)为4mol/L的Cu(NO3)2和AgNO3的混合溶液100mL中,加入一定质量的锌,充分振荡后过滤沉淀,干燥后称量为24.8g,将此沉淀置于稀盐酸中,无气体产生,滤液中先滴加BaCl2溶液无沉淀生成,后加入过量的稀NaOH溶液到沉淀完全,过滤,加热,干燥得4gCuO,求参加反应的锌的物质的量.分析 24.8g是Cu和银的混合物,n(NO3-)=4mol/L×0.1L=0.4mol,根据电荷守恒:2n(Cu2+)+n(Ag+)=0.4mol①
干燥得4gCuO,所以n(CuO)=$\frac{4g}{80g/mol}$=0.05mol,
CuO中n(Cu)=n(CuO)=0.05mol 则混合固体中铜的物质的量为n(Cu2+)-0.05
64[n(Cu2+)-0.05]+108n(Ag+)=24.8 ②
联立①、②,解得n(Cu2+)=0.1mol,n(Ag+)=0.2mol,所以与锌反应的银离子的物质的量为0.2mol,铜离子的物质的量为:0.1-0.05=0.05mol,根据得失电子守恒分析,参加反应的锌的物质的量.
解答 解:24.8g是Cu和银的混合物,n(NO3-)=4mol/L×0.1L=0.4mol,根据电荷守恒:2n(Cu2+)+n(Ag+)=0.4mol①
干燥得4gCuO,所以n(CuO)=$\frac{4g}{80g/mol}$=0.05mol,
CuO中n(Cu)=n(CuO)=0.05mol 则混合固体中铜的物质的量为n(Cu2+)-0.05
64[n(Cu2+)-0.05]+108n(Ag+)=24.8 ②
联立①、②,解得n(Cu2+)=0.1mol,n(Ag+)=0.2mol,所以与锌反应的银离子的物质的量为0.2mol,铜离子的物质的量为:0.1-0.05=0.05mol,所以参加反应锌的物质的量为:$\frac{0.05×2+0.2}{2}$=0.15mol,答:参加反应的锌的物质的量0.15mol.
点评 本题考查混合物有关计算,关键是判断Zn与混合溶液反应的溶液中溶质为Cu(NO3)2、Zn(NO3)2,再利用守恒法解答,利用守恒法可简化计算过程,减少数学计算,侧重考查学生分析计算能力,难度中等.

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案| A. | H3PO4>H2CO3>H2SiO3 | B. | H2CO3>H2SiO3>H3PO4 | ||
| C. | H2SiO3>H3PO4>H2CO3 | D. | H2SiO3>H2CO3>H3PO4 |
| A. | 在浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 | |
| B. | 葡萄糖注射液不产生丁达尔效应,不属于胶体 | |
| C. | 在Fe(0H)3胶体中.H+、K+、S2-、Br-能大量共存 | |
| D. | 明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 |
| A. | NH4+ | B. | Ba2+ | C. | K+ | D. | I- |
| A. |  2-乙基丙烷 2-乙基丙烷 | B. |  间二甲苯 间二甲苯 | ||
| C. | CH3CH2CH2CH2OH 1-丁醇 | D. | 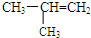 2-甲基-2-丙烯 2-甲基-2-丙烯 |

| A. | 该电池属于二次电池 | |
| B. | 回收该电池,可以获取锂元素,有利于节约资源 | |
| C. | 该电池丢入火中可能引起爆炸 | |
| D. | Li+无毒,该电池可随生活垃圾处理 |
| A. | 小苏打--Na2CO3 | B. | 烧碱--NaOH | C. | 铁红--Fe3O4 | D. | 明矾--KAl(SO4)2 |
| A. | Ba(OH)2 | B. | Ba(NO3)2 | C. | BaC12 | D. | Na2S |