题目内容
3.氯化钠是日常生活的必需品,也是重要的化工原料.粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质.以下是粗盐提纯的操作流程.
提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液、稀盐酸.
(1)欲除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,试剂的选择和滴加顺序均正确的是:CE;
A、Na2CO3溶液、BaCl2溶液、NaOH溶液
B、溶液、NaOH溶液、K2CO3溶液
C、NaOH溶液、BaCl2溶液、Na2CO3溶液
D、Ba(NO3)2、NaOH溶液、Na2CO3溶液
E、BaCl2溶液、Na2CO3溶液、NaOH溶液
(2)过量碳酸盐溶液的作用是除尽钙离子和过量的钡离子.
(3)洗涤晶体操作使用的玻璃仪器有烧杯、漏斗、玻璃棒.
(4)蒸发结晶的操作方法是蒸发过程中不断用玻璃棒搅拌液体防止受热不均,液体飞溅.看到有大量固体析出,或者仅余少量液体时,停止加热,利用余热将液体蒸干.
分析 除去粗盐中的Ca2+、Mg2+、SO42-,可以加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除钙离子和过量的钡离子.加氢氧化钠和氯化钡无先后顺序要求.洗涤晶体操作用到的是过滤那套装置,蒸发结晶在蒸发皿中进行,注意加热时的操作.
解答 解:(1)除去溶液I中的MgCl2、CaCl2、Na2SO4,应考虑到除杂试不引入新的杂质,所以从提供的试剂中选Na2CO3溶液、NaOH溶液、BaCl2溶液,加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除钙离子和过量的钡离子.加氢氧化钠和氯化钡无先后顺序要求.所以可以有的顺序:BaCl2溶液、Na2CO3溶液、NaOH溶液;NaOH溶液、BaCl2溶液、Na2CO3溶液;BaCl2溶液、Na2CO3溶液、NaOH溶液;故CE正确.
故答案为:CE.
(2)加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除钙离子和过量的钡离子.
故答案为:除尽钙离子和过量的钡离子.
(3)洗涤晶体操作用到的是过滤那套装置,用到的玻璃仪器有:烧杯、漏斗、玻璃棒.
故答案为:烧杯、漏斗、玻璃棒
(4)蒸发结晶在蒸发皿中进行,蒸发皿放于铁架台的铁圈上,倒入液体不超过蒸发皿容积的2/3,加热时不断用玻璃棒搅拌液体防止受热不均,液体飞溅.看到有大量固体析出,或者仅余少量液体时,停止加热,利用余热将液体蒸干.
故答案为:加热时不断用玻璃棒搅拌液体防止受热不均,液体飞溅.看到有大量固体析出,或者仅余少量液体时,停止加热,利用余热将液体蒸干.
点评 本题主要考查了除杂质的原则,以及除杂质的顺序,注意为了将杂质除净,每次所加试剂要过量,不引入新的杂质,这类题时常出现,要加以掌握.物质分离提纯的基本实验操作的考查比较简单.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
10.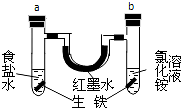 如图装置中,U型管内为红墨水,a、b试管中分别盛有食盐水和氯化铵溶液(已知氯化铵溶液呈酸性),各加入生铁块,放置一段时间.下列有关描述错误的是( )
如图装置中,U型管内为红墨水,a、b试管中分别盛有食盐水和氯化铵溶液(已知氯化铵溶液呈酸性),各加入生铁块,放置一段时间.下列有关描述错误的是( )
 如图装置中,U型管内为红墨水,a、b试管中分别盛有食盐水和氯化铵溶液(已知氯化铵溶液呈酸性),各加入生铁块,放置一段时间.下列有关描述错误的是( )
如图装置中,U型管内为红墨水,a、b试管中分别盛有食盐水和氯化铵溶液(已知氯化铵溶液呈酸性),各加入生铁块,放置一段时间.下列有关描述错误的是( )| A. | a中发生了吸氧腐蚀,b中发生了析氢腐蚀 | |
| B. | a中正极反应方程式是:O2+2H2O+4e-═4OH- | |
| C. | a、b试管中生铁块中铁都作电池的负极 | |
| D. | 红墨水在一段时间后,两边液面变为左低右高 |
7.设NA为阿伏伽德罗常数的值,下列叙述中正确的是( )
| A. | 7.8g N2O2晶体中阴离子数目为0.2NA | |
| B. | 含1mol NH4Cl和少量NH3•H2O的中性溶液中,NH${\;}_{4}^{+}$数目为NA | |
| C. | 电解精炼铜时,阳极质量减少64g外电路导线上通过的e-数目为NA | |
| D. | 室温下,1L pH=13的NaOH溶液中,由水电离的OH-数目为0.1NA |
15.下列说法正确的是( )
| A. | 离子键就是阴、阳离子间的静电引力 | |
| B. | 所有金属元素与所有非金属元素间都能形成离子键 | |
| C. | NH4Cl属于离子化合物 | |
| D. | 在离子化合物CaCl2中,两个氯离子间也存在离子键 |
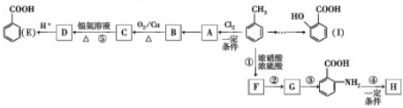
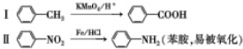
 .
. .写出③的转化关系
.写出③的转化关系 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$ (用已知中的表达式表示,不用写化学方程式)
(用已知中的表达式表示,不用写化学方程式)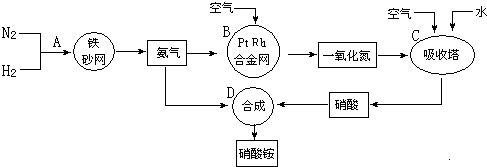
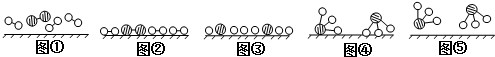
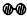 、
、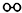 、
、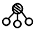 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面、在催化剂表面N2、H2中的化学键断裂.
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面、在催化剂表面N2、H2中的化学键断裂.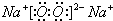 ;B的氢化物的结构式为
;B的氢化物的结构式为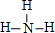 ;
;
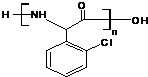 ;D→E所需X物质的结构简式:
;D→E所需X物质的结构简式:
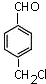 .
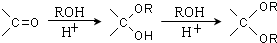
.
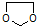 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下: