题目内容
W、Q、R、X、Y均为短周期中五种元素,已知W的低价氧化物分子与R单质分子电子总数相等,相对分子质量也相等;Q与W同族,Q、X、Y同周期,X-、Y2-简单阴离子具有相同电子层结构.请回答:
(1)W原子的结构示意图: ;其最高价氧化物的结构式: .
(2)W最高价氧化物的熔沸点 Q的最高价氧化物溶沸点(填“大于”、“小于”或“等于”);主要原因是 ;
(3)Q与R形成的化合物是一种新型无机非金属材料,其化学式: ;属于 晶体.
(4)1.2gW单质在氧气中充分燃烧放出39.35kJ的能量,请写出该反应的热化学方程式: .
(1)W原子的结构示意图:
(2)W最高价氧化物的熔沸点
(3)Q与R形成的化合物是一种新型无机非金属材料,其化学式:
(4)1.2gW单质在氧气中充分燃烧放出39.35kJ的能量,请写出该反应的热化学方程式:
分析:W、Q、R、X、Y均为短周期中五种元素,W的低价氧化物分子与R单质分子的电子总数以及相对分子质量均相等,可推测W为碳元素,R为氮元素;Q与W同主族,可以确定Q为硅元素;X、Y与Q同周期,且X-、Y2-简单阴离子具有相同电子层结构,可以确定X是氯元素,Y是硫元素,据此解答.
解答:解:W、Q、R、X、Y均为短周期中五种元素,W的低价氧化物分子与R单质分子的电子总数以及相对分子质量均相等,可推测W为碳元素,R为氮元素;Q与W同主族,可以确定Q为硅元素;X、Y与Q同周期,且X-、Y2-简单阴离子具有相同电子层结构,可以确定X是氯元素,Y是硫元素,
(1)W为碳元素,其原子的结构示意图为: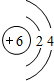 ;其最高价氧化物的结构式为:O=C=O,
;其最高价氧化物的结构式为:O=C=O,
故答案为: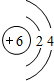 ;O=C=O;
;O=C=O;
(2)CO2是分子晶体,SiO2是原子晶体,故熔沸点CO2<SiO2,
故答案为:小于;晶体类别不同,CO2是分子晶体,SiO2是原子晶体;
(3)Si与N形成的化合物是一种新型无机非金属材料,其化学式为:Si3N4,属于原子晶体,
故答案为:Si3N4;原子;
(4)1.2g碳单质的物质的量为0.1mol,在氧气中充分燃烧放出39.35kJ的能量,故1mol碳单质完全反应放出的热量为393.5kJ,该反应的热化学方程式为:C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol-1,
故答案为:C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol-1.
(1)W为碳元素,其原子的结构示意图为:
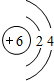 ;其最高价氧化物的结构式为:O=C=O,
;其最高价氧化物的结构式为:O=C=O,故答案为:
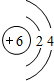 ;O=C=O;
;O=C=O;(2)CO2是分子晶体,SiO2是原子晶体,故熔沸点CO2<SiO2,
故答案为:小于;晶体类别不同,CO2是分子晶体,SiO2是原子晶体;
(3)Si与N形成的化合物是一种新型无机非金属材料,其化学式为:Si3N4,属于原子晶体,
故答案为:Si3N4;原子;
(4)1.2g碳单质的物质的量为0.1mol,在氧气中充分燃烧放出39.35kJ的能量,故1mol碳单质完全反应放出的热量为393.5kJ,该反应的热化学方程式为:C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol-1,
故答案为:C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol-1.
点评:本题考查结构性质位置关系应用,推断元素是解题的关键,需要学生熟练掌握基础知识,难度中等.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
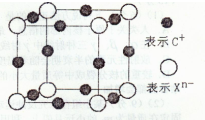
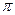 键。
键。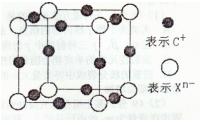
 键。
键。