题目内容
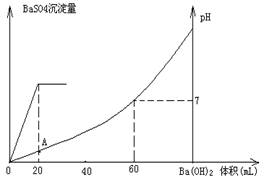
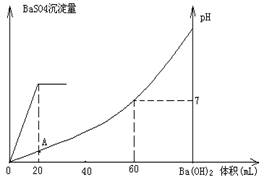
硫酸和盐酸混合溶液20mL,加入0.05mol/L的Ba(OH)2溶液时,生成BaSO4沉淀量及溶液pH发生下图所示的变化。
⑴开始时混合溶液中硫酸和盐酸的物质的量浓度各是多少?
⑵在A点溶液的pH是多少?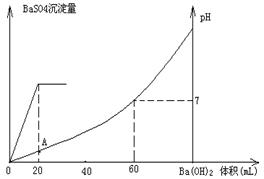
(1)关键图像可判断和硫酸反应的氢氧化钡是20ml,和盐酸反应的氢氧化钡是40ml。氢氧化钡和硫酸反应的方程式为:H2SO4+Ba(OH)2=2H2O+BaSO4↓
1mol 1mol
0.02L×c 0.02L×0.05mol/L
因此c=0.05mol/L
盐酸和氢氧化钡反应的方程式为:Ba(OH)2+2HCl=BaCl2+2H2O
_ 1mol 2mol
_ 0.04L×0.05mol/L 0.02L×c
所以c=0.20mol/L
(2)在A点硫酸恰好反应,溶液中只有盐酸,此时溶液的体积是40ml,所以溶液中氢离子
浓度为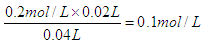 ,所以pH=1.0
,所以pH=1.0
解析

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
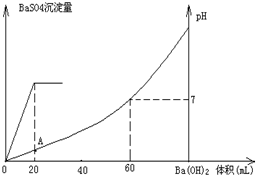 常温下,向20mL硫酸和盐酸混合溶液中加入0.05mol/L的Ba(OH)2溶液时,生成BaSO4沉淀量及溶液pH发生如图所示的变化.
常温下,向20mL硫酸和盐酸混合溶液中加入0.05mol/L的Ba(OH)2溶液时,生成BaSO4沉淀量及溶液pH发生如图所示的变化.