题目内容
(6分)氯化铜晶体(CuCl2·2H2O)含有FeCl2杂质,为制得纯净氯化铜晶体,首先将其制成水溶液,然后按下列操作步骤进行提纯:
①先加入氧化剂X,再加入物质Y,过滤得沉淀Z;
②将滤液蒸发结晶得纯CuCl2·2H2O晶体。
已知:三种离子从溶液中完全呈氢氧化物沉淀所需pH值:Fe3+:3.7,Cu2+:6.4,Fe2+:6.4试回答下列问题:
(1)加入氧化剂X的原因是____ __。
(2)下列物质都可以作为氧化剂,其中最适宜于本实验的是( )
A.H2O2 B.KMnO4 C.NaClO D.K2CrO7
(3)物质Y是__ ____,沉淀Z是__ ____.
(4)为分离出沉淀Z,采取的实验操作所用仪器有__ ____。
(5)操作②所用的仪器有____ __。
(6分,每空1分)
(1)把Fe2+氧化为Fe3+便于分离提纯CuCl2; (2)A;
(3)CuO,Fe(OH)3 (4)漏斗、铁架台、铁圈、烧杯、玻璃棒、滤纸
(5)蒸发皿、三角架(或铁架台、铁圈)酒精灯、玻璃棒
【解析】
试题分析:(1)Fe2+氧化为Fe3+,易生成氢氧化铁沉淀而除去,以便得到纯净的氯化铜。
(2)加入氧化剂X可把Fe2+氧化为Fe3+,而没有增加新杂质,所以X为H2O2,故答案为:A。
(3)结合题示,调节pH至4~5,使Fe3+全部沉淀,同样不引进新杂质,所以Y最好为CuO或Cu(OH)2或CuCO3,得到的沉淀为Fe(OH)3。
(4)为分离出沉淀Z,应用过滤的操作,所使用的仪器为漏斗、铁架台、铁圈、烧杯、玻璃棒、滤纸等。
(5)操作②为蒸发操作,所使用的仪器有蒸发皿、三角架(或铁架台、铁圈)酒精灯、玻璃棒
考点:本题考查实验基本仪器和基本操作、实验方案的设计。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案

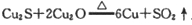 反应中,说法正确的是( )
反应中,说法正确的是( )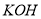 溶液中,得到含有次氯酸钾、氯酸钾和氯化钾的混合溶液。若反应过程中转移
溶液中,得到含有次氯酸钾、氯酸钾和氯化钾的混合溶液。若反应过程中转移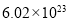 个电子,所得溶液中
个电子,所得溶液中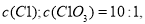 则参与反应的
则参与反应的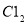 的物质的量为
的物质的量为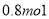 B.
B.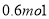 C.
C.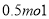 D.
D.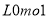
 CO2(g)+H2(g)
CO2(g)+H2(g)
 CO2(g)+H2(g)达到平衡状态的是_________
CO2(g)+H2(g)达到平衡状态的是_________ (CO)=
(CO)= (CO)=_____;
(CO)=_____; (填“>”或“<”),平衡向__________方向移动(填“正反应”、“逆反应”“不移动”)
(填“>”或“<”),平衡向__________方向移动(填“正反应”、“逆反应”“不移动”)