题目内容
7.6.4g铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、NO的混合气体nL(标准状况),这些气体与一定体积O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,则消耗O2的体积为多少?分析 Cu与硝酸反应生成硝酸铜、NO2、NO的混合气体,生成的NO2、NO 的混合气体与O2(标准状况)混合后通入水中,所有气体完全被水吸收又生成硝酸,纵观整个过程,由电子转移守恒,可知Cu提供电子等于氧气获得的电子,进而计算消耗氧气体积.
解答 解:Cu与硝酸反应生成硝酸铜、NO2、NO的混合气体,生成的NO2、NO 的混合气体与O2(标准状况)混合后通入水中,所有气体完全被水吸收又生成硝酸,纵观整个过程,由电子转移守恒,可知Cu提供电子等于氧气获得的电子,Cu失去电子为$\frac{6.4g}{64g/mol}$×2=0.2mol,故消耗氧气为$\frac{0.2mol}{4}$=0.05mol,标况下消耗氧气体积为0.05mol×22.4L/mol=1.12L,
答:消耗氧气体积为1.12L.
点评 本题考查氧化还原反应计算,难度中等,侧重考查学生的分析思维能力与解题方法技巧,注意利用守恒法进行解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.下列试剂不会因为空气中的氧气而变质的是( )
| A. | 亚硫酸钠 | B. | 过氧化钠 | C. | 硫酸亚铁 | D. | 氢硫酸 |
2.某同学拟设计如下流程测定铜银合金中铜的质量分数:
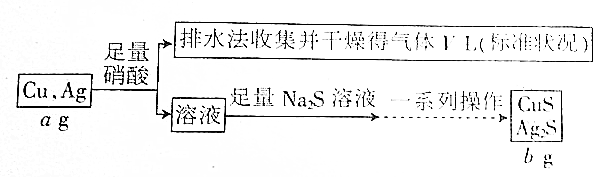
下列说法不正确的是( )

下列说法不正确的是( )
| A. | V L气体是NO | |
| B. | 一系列操作指“过滤、洗涤、烘干” | |
| C. | 上述数据之间的关系有b=$\frac{7a+15v}{7}$ | |
| D. | 根据上述数据能计算合金中铜的质量分数 |
9.反应3H2+N2?2NH3在密闭容器中进行.下列关于该反应的说法错误的是( )
| A. | 升高温度能加快反应速率 | B. | 使用恰当的催化剂能加快反应速率 | ||
| C. | 将氨气液化排出能加快反应速率 | D. | N2与H2不能完全转化为NH3 |
7.下列实验操作错误的是( )
| A. | 为防止试管破裂,加热固体碳酸氢钠时,试管口应略向下倾斜 | |
| B. | 为防止液体暴沸,蒸馏时可在烧瓶中加入少量碎瓷片 | |
| C. | 容量瓶可用于配制一定物质的量浓度的溶液,不可作为反应容器使用 | |
| D. | 配制500mL 0.1 mol/L NaOH溶液时,将2g NaOH固体倒入500mL容量瓶中,加水至凹液面与刻度线相切 |
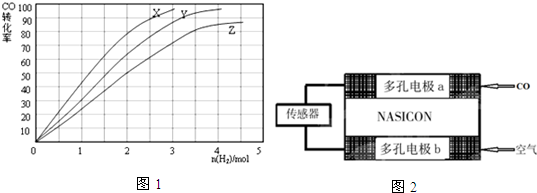

 ,实验中,可以观察到反应②的现象是:气体由无色变红棕色.
,实验中,可以观察到反应②的现象是:气体由无色变红棕色.