题目内容
4.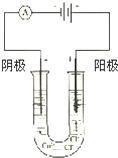 按如图所示装置连接好仪器在U形管中加入饱和氯化铜溶液,用石墨棒作电极,接通电源,电解数分钟后,观察现象.
按如图所示装置连接好仪器在U形管中加入饱和氯化铜溶液,用石墨棒作电极,接通电源,电解数分钟后,观察现象.(1)接电源负极的石墨棒上现象析出红色金属
(2)阳极电极反应为2Cl--2e-=Cl2↑,电解反应的化学方程式CuCl2$\frac{\underline{\;电解\;}}{\;}$Cu+Cl2↑
(3)在上述电解反应中,被氧化的物质是氯离子(填“氯”或“铜”)
分析 电解氯化铜溶液,阳极发生氧化反应生成氯气,电极方程式为2Cl--2e-=Cl2↑,阴极发生还原反应生成铜,电极方程式为Cu2++2e-=Cu,以此解答该题.
解答 解:(1)接电源负极的石墨棒为阴极,发生Cu2++2e-=Cu,可观察到阴极析出铜,为红色金属,故答案为:析出红色金属;
(2)阳极发生氧化反应生成氯气,电极方程式为2Cl--2e-=Cl2↑,电解总反应式为CuCl2$\frac{\underline{\;电解\;}}{\;}$Cu+Cl2↑,
故答案为:2Cl--2e-=Cl2↑;CuCl2$\frac{\underline{\;电解\;}}{\;}$Cu+Cl2↑;
(3)阳极发生氧化反应生成氯气,被氧化的为氯离子,故答案为:氯.
点评 本题考查电解原理,为高频考点,侧重于学生的分析能力的考查,明确各个电极上发生的反应是解本题关键,难点是电极反应式的书写,题目难度不大.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
14.只需加入一种试剂就可以把Na2SiO3、Na2CO3、MgCl2、Ba(HCO3)2四种无色溶液鉴别出来,这种试剂是( )
| A. | 盐酸 | B. | 硫酸 | C. | 石灰水 | D. | 硝酸银溶液 |
12.下列说法正确的是( )
| A. | 增加反应物的用量一定能增大反应速率 | |
| B. | 化学反应速率只能加快不能减慢 | |
| C. | 决定化学反应速率的主要因素是浓度 | |
| D. | 参加反应物质的性质是决定化学反应速率的主要因素 |
19.NM-3是处于临床试验阶段的小分子抗癌药物,分子结构如图.下列说法正确的是( )


| A. | 该有机物的化学式为C12H12O6 | |
| B. | 1mol该有机物最多可以和3molNaOH反应 | |
| C. | 该有机物容易发生加成、取代、消去等反应 | |
| D. | 该有机物可代替KSCN检验Fe3的存在 |
9. 将烧喊吸收H2S后的溶液加入到如图所示的电解池的阳极区进行电解,以实现H2S转化为S的目的.下列判断错误的是( )
将烧喊吸收H2S后的溶液加入到如图所示的电解池的阳极区进行电解,以实现H2S转化为S的目的.下列判断错误的是( )
 将烧喊吸收H2S后的溶液加入到如图所示的电解池的阳极区进行电解,以实现H2S转化为S的目的.下列判断错误的是( )
将烧喊吸收H2S后的溶液加入到如图所示的电解池的阳极区进行电解,以实现H2S转化为S的目的.下列判断错误的是( )| A. | 电解过程中阳极区发生如下反应:S2--2e-=S,(n-l)S+S2-=Sn2- | |
| B. | 电解时阴极的电极反应式:2H20+2e-═H2↑+20H- | |
| C. | 电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成Sn2-+2H+═nS↓+H2↑ | |
| D. | 该装置的离子交换膜为阳离子交换膜 |
13.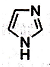 离子液体在有机合成、无机合成等方面有着重要应用.咪唑是合成“离子液体”的一种原料,其结构如图所示.下列有关咪唑说法不正确的是( )
离子液体在有机合成、无机合成等方面有着重要应用.咪唑是合成“离子液体”的一种原料,其结构如图所示.下列有关咪唑说法不正确的是( )
 离子液体在有机合成、无机合成等方面有着重要应用.咪唑是合成“离子液体”的一种原料,其结构如图所示.下列有关咪唑说法不正确的是( )
离子液体在有机合成、无机合成等方面有着重要应用.咪唑是合成“离子液体”的一种原料,其结构如图所示.下列有关咪唑说法不正确的是( )| A. | 化学式C3H4N2 | |
| B. | 分子中含有一种非极性键和两种极性键 | |
| C. | 可以发生取代、加成、氧化反应 | |
| D. | 一氯取代物的同分异构体共有4种 |
18.用已知浓度的NaOH滴定未知浓度的盐酸,下列操作(其他操作正确)会造成测定结果偏高的是( )
| A. | 滴定终点读数时俯视度数 | |
| B. | 酸式滴定管使用前,水洗后未用待测盐酸润洗 | |
| C. | 锥形瓶洗净后未干燥 | |
| D. | 碱式滴定管滴定前尖嘴部分有气泡,滴定后气泡消失 |
 .
.