题目内容
下列化合物分子中一定既含单键又含双键的是( )
| A、CO2 |
| B、H2O2 |
| C、C2H2 |
| D、COCl2 |
考点:共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:分子中形成1对共用电子对,则为单键;若两原子之间形成2对共用电子对,则为双键,以此来解答.
解答:
解:A.只含C=O键,则只有双键,故A不选;
B.只有H-O、O-O键,则只有单键,故B不选;
C.含C-H、C≡C,则不含双键,故C不选;
D.含C=O、C-Cl,所以既含单键又含双键,故D选;
故选D.
B.只有H-O、O-O键,则只有单键,故B不选;
C.含C-H、C≡C,则不含双键,故C不选;
D.含C=O、C-Cl,所以既含单键又含双键,故D选;
故选D.
点评:本题考查化学键,为高频考点,把握化学键判断的一般规律为解答的关键,注重基础知识的考查,注意物质结构中的化学键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某离子化合物的晶胞如图所示立体结构,晶胞是整个晶体中最基本的重复单位.小黑球表示阳离子,小白球表示阴离子,该离子化合物中,阴、阳离子个数比是( )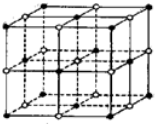

| A、1:8 | B、1:4 |
| C、1:2 | D、1:1 |
相同状态下,10体积A2气体和20体积B2气体化合成20体积气体C,则C的化学式为( )
| A、AB |
| B、A2B |
| C、AB3 |
| D、AB2 |
下列各组离子一定能大量共存的是( )
| A、在含有大量[Al(OH)4]-的溶液中:NH4+、Na+、Cl-、H+ |
| B、在c(H+)=0.1mol?L-1的溶液中:K+、I-、Cl-、NO3- |
| C、在pH=12的溶液中:NH4+、Na+、SO42-、Cl- |
| D、在强碱溶液中:Na+、K+、CO32-、NO3- |
能在水溶液中大量共存的离子组是( )
| A、Cu2+ Fe2+ ClO-Cl- |
| B、Na+、Al3+、NO3-、CO32- |
| C、K+ AlO2-Cl- OH- |
| D、Mg2+、H+、Br-、HCO3- |
已知NA为阿伏伽德罗常数,下列说法不正确的是( )
| A、醋酸的摩尔质量与NA个醋酸分子的质量当以克为单位时在数值上相等 |
| B、22g二氧化碳与11.2L的HCl含有相同的分子数 |
| C、常温常压下,17gNH3所含有的原子数为4NA |
| D、500mL 0.2mol?L-1的Ba(NO3)2溶液中NO3-的物质的量浓度为0.4mol?L-1 |
下列有关物质组成与结构表示方法不正确的是( )
A、HClO 电子式: | ||
B、CH4 比例模型: | ||
| C、乙炔结构简式:HC≡CH | ||
D、质子数55,中子数82的原子
|
设阿伏加德罗常数为NA,则下列说法正确的是( )
| A、常温常压下,3.2 g O2和O3的混合气中氧原子数为0.2NA |
| B、1L2mol?L-1 K2S溶液中S2-和HS-的总数为2NA |
| C、标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
| D、50mL18mol?L-1浓硫酸与足量铜微热反应,转移的电子数为1.8NA |