题目内容
结构决定性质是化学科学中一个基本规律.主族非金属元素的氢化物在结构和性质各有特点.
(1)化学键的偶极矩是矢量,方向规定为从正电中心指向负电中心,方向用→表示.甲烷和甲硅烷的偶极矩如图1所示,那么H、C、Si电负性由大到小的顺序是 .
(2)分子的极性大小与分子的空间构型及化学键的极性大小有关,物质结构上常用偶极矩表示分子极性的大小.下表是常见氢化物的偶极矩(μ)数据:
据此分析:①μ(甲烷)=0的原因是:
②μ(水)>μ(硫化氢)的原因是:
(3)NH3、H2O都可以作为配体,形成配合物,CH4不能做配体,原因是
(4)叠氮酸HN3的结构式如图2所示,其中①号N的杂化方式为 ,②号N的杂化方式为 .预测其在水中的溶解度 (填写“大”或“小”)
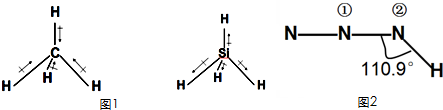
(1)化学键的偶极矩是矢量,方向规定为从正电中心指向负电中心,方向用→表示.甲烷和甲硅烷的偶极矩如图1所示,那么H、C、Si电负性由大到小的顺序是
(2)分子的极性大小与分子的空间构型及化学键的极性大小有关,物质结构上常用偶极矩表示分子极性的大小.下表是常见氢化物的偶极矩(μ)数据:
| 物质 | 甲烷 | 氨气 | 水 | 硫化氢 |
| 偶极矩(μ)/德拜尔 | 0 | 1.66 | 1.85 | 1.1 |
②μ(水)>μ(硫化氢)的原因是:
(3)NH3、H2O都可以作为配体,形成配合物,CH4不能做配体,原因是
(4)叠氮酸HN3的结构式如图2所示,其中①号N的杂化方式为

考点:物质的组成、结构和性质的关系,元素电离能、电负性的含义及应用,原子轨道杂化方式及杂化类型判断
专题:
分析:(1)根据共用电子对偏向电负性大的原子进行解答.
(2)①甲烷是正四面体结构,偶极矩相互抵消;
②据O的电负性大于S来分析;
(3)NH3、H2O均有孤对电子,都可以作为配体,但CH4无孤对电子;
(4)①号N含1条S轨道和1条P轨道杂化使形成的N-N键角为180°,符合SP1杂化理论;在HN3分子中,三个N原子以直线相连,H-N键与N-N-N键间的夹角为110°9',显然靠近H原子的第1个N原子是sp2杂化的.
(2)①甲烷是正四面体结构,偶极矩相互抵消;
②据O的电负性大于S来分析;
(3)NH3、H2O均有孤对电子,都可以作为配体,但CH4无孤对电子;
(4)①号N含1条S轨道和1条P轨道杂化使形成的N-N键角为180°,符合SP1杂化理论;在HN3分子中,三个N原子以直线相连,H-N键与N-N-N键间的夹角为110°9',显然靠近H原子的第1个N原子是sp2杂化的.
解答:
解:(1)共用电子对偏向电负性大的原子,CH4中共用电子对偏向C,则电负性C>H;SiH4中共用电子对偏向H,则电负性H>Si,所以C、Si、H的电负性大小关系为:C>H>Si,故答案为:C>H>Si;
(2)①甲烷是正四面体结构,偶极矩相互抵消,为非极性分子,故μ(甲烷)=0,故答案为:CH4是正四面体构型,为非极性分子;
②O的电负性大于S,所以O-H的极性大于S-H,故μ(水)>μ(硫化氢),故答案为:O的电负性大于S,所以O-H的极性大于S-H;
(3)NH3、H2O均有孤对电子,都可以作为配体,但CH4无孤对电子,不能做配体,故答案为:CH4没有孤对电子而NH3中的N,H2O中的O都有孤对电子;
(4)①号N含1条S轨道和1条P轨道杂化使形成的N-N键角为180°,符合SP1杂化理论,故①号N是SP1杂化;在HN3分子中,三个N原子以直线相连,H-N键与N-N-N键间的夹角为110°9',显然靠近H原子的第1个N原子是sp2杂化的;由于叠氮酸是极性分子,根据相似相溶原理,故在水中的溶解度较大,故答案为:sp1;sp2;大.
(2)①甲烷是正四面体结构,偶极矩相互抵消,为非极性分子,故μ(甲烷)=0,故答案为:CH4是正四面体构型,为非极性分子;
②O的电负性大于S,所以O-H的极性大于S-H,故μ(水)>μ(硫化氢),故答案为:O的电负性大于S,所以O-H的极性大于S-H;
(3)NH3、H2O均有孤对电子,都可以作为配体,但CH4无孤对电子,不能做配体,故答案为:CH4没有孤对电子而NH3中的N,H2O中的O都有孤对电子;
(4)①号N含1条S轨道和1条P轨道杂化使形成的N-N键角为180°,符合SP1杂化理论,故①号N是SP1杂化;在HN3分子中,三个N原子以直线相连,H-N键与N-N-N键间的夹角为110°9',显然靠近H原子的第1个N原子是sp2杂化的;由于叠氮酸是极性分子,根据相似相溶原理,故在水中的溶解度较大,故答案为:sp1;sp2;大.
点评:本题考查了叠氮酸的结构以及杂化方式和电负性的比较,难度不大.

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
下列叙述Ⅰ和Ⅱ均正确并有因果关系的是( )
| A、较强酸可制较弱酸,次氯酸无法制盐酸 |
| B、Ca(OH)2能制成澄清石灰水,次氯酸无法制盐酸 |
| C、KNO3的溶解度大,用重结晶法除去KNO3中混有的NaCl |
| D、BaSO4难溶于酸,用盐酸和BaCl2溶液检验SO42- |
某同学探究氨和铵盐的性质,相关实验操作及现象描述正确的是( )
| A、加热NH4Cl晶体制备氨气 |
| B、将蘸有浓氨水和浓硝酸的玻璃棒靠近,观察到白烟 |
| C、将氨水缓慢滴入AlCl3溶液中,研究Al(OH)3的两性 |
| D、室温下测定等浓度氨水和NaOH溶液的pH,比较N和Na的金属性强弱 |
下列关于化学反应速率的说法正确的是( )
| A、化学反应速率可用一定时间内任何一种反应物浓度的减小或生成物浓度的增加来表示 |
| B、化学反应速率0.8mol?L-1?s-1是指1s时某物质的浓度为0.8mol?L-1 |
| C、根据化学反应速率可以知道化学反应进行的快慢 |
| D、对于任何化学反应来说,反应速率越大,反应现象就越明显 |
如图所示,由锌片、铜片和稀硫酸溶液构成的原电池中,下列叙述正确的是( )
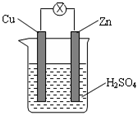

| A、锌片为负极,发生还原反应 |
| B、电流从锌片流向铜片 |
| C、一段时间后,铜片质量减轻 |
| D、一段时间后,溶液pH值变大 |
下列各溶液中,Na+浓度最大的是( )
| A、0.8L 0.4mol/L的NaOH溶液 |
| B、0.1L 0.5mol/L的NaCl溶液 |
| C、1L 0.3mol/L的NaCl溶液 |
| D、0.2L0.25mol/L的Na3PO4溶液 |
下列不属于物理量的是( )
| A、物质的量 | B、摩尔 |
| C、阿伏伽德罗常数 | D、物质的量浓度 |