题目内容
下列分子或离子之间互为等电子体的是( )
| A、CCl4和PO43- |
| B、NH3和NH4+ |
| C、NO2和CS2 |
| D、CO2和SO2 |
考点:“等电子原理”的应用
专题:原子组成与结构专题
分析:原子总数和价电子总数相同的分子或离子称为等电子体,等电子体间结构和性质相似(等电子原理).
解答:
解:A、CCl4和PO43-离子中均含有5个原子,32个价电子,所以是等电子体,故A正确;
B、分子含有4个原子,NH4+离子含有5个原子,所以不是等电子体,故B错误;
C、NO2分子含有3个原子,17个价电子;CS2含有3个原子,16个价电子数,所以不是等电子体,故C错误;
D、CO2分子中都含有3个原子,16个价电子;SO2分子中含有3个原子,18个价电子数,所以不是等电子体,故D错误;
故选:A.
B、分子含有4个原子,NH4+离子含有5个原子,所以不是等电子体,故B错误;
C、NO2分子含有3个原子,17个价电子;CS2含有3个原子,16个价电子数,所以不是等电子体,故C错误;
D、CO2分子中都含有3个原子,16个价电子;SO2分子中含有3个原子,18个价电子数,所以不是等电子体,故D错误;
故选:A.
点评:本题考查等电子体的判断,根据等电子体的定义来分析解答即可,难度不大.

练习册系列答案
相关题目
 如图是a、b两种固体物质的溶解度曲线.下列说法中正确的是( )
如图是a、b两种固体物质的溶解度曲线.下列说法中正确的是( )| A、a物质的溶解度受温度变化的影响较小,b物质的溶解度受温度变化的影响较大 |
| B、t℃时,等质量的a、b饱和溶液中含有相同质量的溶质 |
| C、当温度大于t℃时,a溶液一定比b溶液浓 |
| D、a中含有少量b时,用冷却热饱和溶液的方法提纯a |
下列说法正确的是( )
| A、摩尔是用于描述微观粒子的物理量 |
| B、0.012kg12C所含的原子数精确值是6.02×1023 |
| C、1mol H2的体积为22.4L |
| D、1molH2SO4的质量是98g |
下列离子方程式正确的是( )
| A、饱和碳酸钠溶液中通入过量的CO2:CO32-+H2O+CO2=2HCO3- |
| B、氯气跟水反应:Cl2+H2O=2H++Cl-+ClO- |
| C、过氧化钠投入水中:Na2O2+H2O=2Na++2OH-+O2↑ |
| D、氯化铝溶液中加入过量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
海藻中含有丰富的碘元素.下图是实验室从海藻里提取碘的流程的一部分.下列判断正确的是( )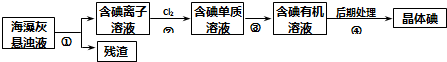

| A、步骤④的操作是过滤 |
| B、可用淀粉溶液检验步骤②的反应是否进行完全 |
| C、步骤①、③的操作分别是过滤、萃取 |
| D、步骤③中加入的有机溶剂可能是苯或CCl4 |
正硼酸(H3BO3)是一种片层状结构白色晶体,受热易分解.层内的 H3BO3分子通过氢键相连(如图所示),则下列有关说法中正确的是( )
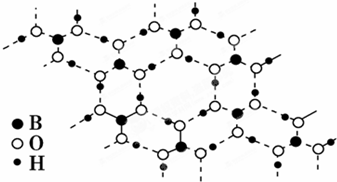

| A、正硼酸晶体属于原子晶体 |
| B、H3BO3分子的稳定性与氢键有关 |
| C、1 mol H3BO3晶体中含有3 mol氢键 |
| D、分子中硼原子最外层为8电子稳定结构 |
下列离子方程式与所述事实不相符的是( )
| A、苯酚钠溶液中通入少量CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3- | ||
| B、在碳酸氢钠溶液中加入过量的氢氧化钡溶液:Ba2++OH-+HCO3-═BaCO3↓+H2O | ||
C、用新制的氢氧化铜悬浊液检验乙醛中的醛基:CH3CHO+2Cu(OH)2+OH-
| ||
| D、向Ca(ClO)2溶液中通入过量SO2:Ca2++2ClO-+SO2+H2O=CaSO4↓+2H++Cl-+HClO |



