题目内容
15.氧化还原反应中实际上包含氧化和还原两个过程.下面是一个还原过程的反应式:NO3-+4H++3e→NO+2H2O,现有KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生.(1)写出并配平该氧化还原反应的方程式:14HNO3+3Cu2O=6Cu(NO3)2+2NO↑+7H2O.
(2)反应中若产生0.2mol气体,则转移电子的物质的量是0.6mol.
(3)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是:使用了较浓的硝酸,产物中有部分二氧化氮生成.
分析 (1)要使硝酸根离子发生还原反应,则需要加入还原剂,根据给予物质的性质判断;
(2)根据NO和转移电子之间的关系式计算;
(3)被还原硝酸的物质的量增加,说明每摩尔硝酸根离子得电子数减少.
解答 解:(1)要使硝酸根离子发生还原反应,则需要加入还原剂,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中KMnO4、Fe2(SO4)3具有强氧化性,Na2CO3没有氧化性和还原性,Cu2O有还原性,所以能使硝酸根离子发生还原反应的是Cu2O,二者反应生成硝酸铜、NO和水,反应方程式为14HNO3+3Cu2O=6Cu(NO3)2+2NO↑+7H2O,
故答案为:14HNO3+3Cu2O=6Cu(NO3)2+2NO↑+7H2O;
(2)反应中若产生0.2mol气体,则转移电子的数=0.2mol×(5-2)mol=0.6mol,故答案为:0.6;
(3)被还原硝酸的物质的量增加,说明每摩尔硝酸根离子得电子数减少,则生成的气体是二氧化氮,故答案为:使用了较浓的硝酸,产物中有部分二氧化氮生成.
点评 本题考查氧化还原反应,为高考常见题型,注意把握元素的化合价及反应中的变化为解答的关键,侧重基本概念和转移电子数的考查,题目难度不大.

练习册系列答案
相关题目
5.下列说法正确的是( )
| A. | 阳离子只有氧化性,阴离子只有还原性 | |
| B. | 阴极发生还原反应,正极亦发生还原反应 | |
| C. | Cl2与碱溶液的反应,实质是HClO与OH-的反应 | |
| D. | 从氯水中分离出HClO,可加入CaCO3蒸馏 |
6.在密闭容器中进行反应:X2(g)+Y2(g)?2Z(g)已知X2、Y2、Z的起始浓度分别为0.1mol•L-1、0.3mol•L-1、0.2mol•L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A. | Y2为0.15mol/L | B. | Z为0.2mol/L | C. | X2为0.3mol/L | D. | Z为0.4mol/L |
3.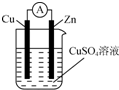 将锌棒和铜棒按图示方式插入CuSO4溶液中,电流计指针发生偏转,下列针对该装置的说法正确的是( )
将锌棒和铜棒按图示方式插入CuSO4溶液中,电流计指针发生偏转,下列针对该装置的说法正确的是( )
 将锌棒和铜棒按图示方式插入CuSO4溶液中,电流计指针发生偏转,下列针对该装置的说法正确的是( )
将锌棒和铜棒按图示方式插入CuSO4溶液中,电流计指针发生偏转,下列针对该装置的说法正确的是( )| A. | 该装置是将电能转化为化学能 | |
| B. | 锌棒为正极 | |
| C. | 电子由铜棒流出 | |
| D. | 该电池总反应为Zn+CuSO4═ZnSO4+Cu |
10.A、B、C、D、E 是同一短周期的五种元素,A和B的最高价氧化物对应的水化物呈碱性,且碱性A强于B,C和D的最高价氧化物的水溶液呈酸性,且酸性C强于D,五种元素形成的简单离子中,E的离子半径最小,则它们的原子序数由大到小的顺序( )
| A. | CDEBA | B. | ECDAB | C. | BAEDC | D. | CDBAE |
20.能证明某溶液中含有Fe2+的是( )
| A. | 该溶液呈浅绿色 | |
| B. | 该溶液中加入NaOH溶液,生成白色沉淀并迅速变成灰绿色,最终变为红褐色 | |
| C. | 向该溶液中加入氯水,再滴入几滴KSCN溶液,呈红色 | |
| D. | 向该溶液中滴入几滴KSCN溶液,不变色,再加入氯水,有红色沉淀生成 |
7.某化学研究性学习小组拟对一种焰火原料(由两种短周期的常见金属单质Li,Na,Mg,Al组成的合金粉末)进行探究.请完成下列探究报告.
【探究目的】探究该焰火原料的组成
【资料检索】①Mg2+检验方法:取2滴待检液,加入2滴2mol•L-1NaOH溶液,再加入1滴镁试剂(Ⅰ)染料(对硝基苯偶氮苯二酚).若出现沉淀并吸附镁试剂(Ⅰ)染料呈天蓝色,表示待检液中含有Mg2+.但Ag+、Cu2+、Fe3+、NH4+会妨碍Mg2+检出
②Mg(OH)2可溶于浓的氯化铵溶液,其他的常见不溶碱难溶于氯化铵
③很多合金是金属互化物,有确定的化学组成
【探究思路】①确定焰火原料所含金属种类;②测定焰火原料的化学式
【实验探究】(1)甲同学进行了初步试验,实验步骤和实验现象如下.请填写下表.
(2)乙同学取甲第②组实验的溶液,加入镁试剂(Ⅰ)染料,得出合金中不含镁.乙的结论错误(选填“正确”或“错误”),你的理由是由资料知,反应必须在碱性条件下进行.
(3)丙同学设计实验方案,确定焰火原料中的金属种类,实验记录如下.
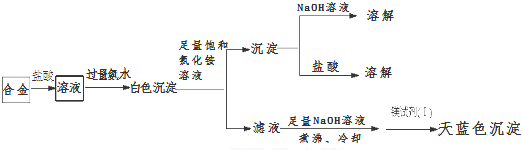
由丙的实验记录可知,该焰火原料是由Mg和Al两种金属组成的合金;实验中滤液加入足量氢氧化钠溶液后需煮沸,煮沸的理由是将NH4+转化为NH3,煮沸促进氨气逸出,防止NH4+干扰Mg2+的检验.
(4)丁同学利用丙同学的结论,设计如下图所示的实验步骤,确定合金组成.

问题讨论:
①能确定合金组成的数据组有a、b、c(填写选项字母);
A.m、n B.m、y C.n、y
②若合金中相对原子质量较小的金属的物质的量分数为x,金属总物质的量为7mol,试在右图中作出y随x变化的曲线;
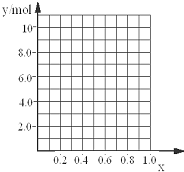
③当y=8.5mol时,该合金是一种金属互化物,其化学式为Mg4Al3.
【探究目的】探究该焰火原料的组成
【资料检索】①Mg2+检验方法:取2滴待检液,加入2滴2mol•L-1NaOH溶液,再加入1滴镁试剂(Ⅰ)染料(对硝基苯偶氮苯二酚).若出现沉淀并吸附镁试剂(Ⅰ)染料呈天蓝色,表示待检液中含有Mg2+.但Ag+、Cu2+、Fe3+、NH4+会妨碍Mg2+检出
②Mg(OH)2可溶于浓的氯化铵溶液,其他的常见不溶碱难溶于氯化铵
③很多合金是金属互化物,有确定的化学组成
【探究思路】①确定焰火原料所含金属种类;②测定焰火原料的化学式
【实验探究】(1)甲同学进行了初步试验,实验步骤和实验现象如下.请填写下表.
| 试验序号 | 实 验 步 骤 | 实 验 现 象 | 结 论 |
| ① | 取少量该焰火原料加入冷水 | 无明显现象 | 不含Li、Na等活泼金属 |
| ② | 取少量该焰火原料加入稀盐酸 | 完全溶解,有大量气体产生,溶液呈无色 | 可能含铍(Be)、镁(Mg)、铝(Al)三种金属中的任意两种 |
(3)丙同学设计实验方案,确定焰火原料中的金属种类,实验记录如下.

由丙的实验记录可知,该焰火原料是由Mg和Al两种金属组成的合金;实验中滤液加入足量氢氧化钠溶液后需煮沸,煮沸的理由是将NH4+转化为NH3,煮沸促进氨气逸出,防止NH4+干扰Mg2+的检验.
(4)丁同学利用丙同学的结论,设计如下图所示的实验步骤,确定合金组成.

问题讨论:
①能确定合金组成的数据组有a、b、c(填写选项字母);
A.m、n B.m、y C.n、y
②若合金中相对原子质量较小的金属的物质的量分数为x,金属总物质的量为7mol,试在右图中作出y随x变化的曲线;

③当y=8.5mol时,该合金是一种金属互化物,其化学式为Mg4Al3.
4.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 7.8 g Na2O2与足量水反应转移的电子数为0.2NA | |
| B. | 常温常压下,1 mol CH4中含有的氢原子数为4NA | |
| C. | 5.6 g铁粉与硝酸反应失去的电子数一定为0.3NA | |
| D. | 12.0 g熔融的NaHSO4中含有0.1NA个Na+、0.1NA个H+和0.1NA个SO42- |
5.下表是元素周期表的一部分,回答下列问题:
(1)写出①、②两种元素的名称碳,氮;⑧、⑨两种元素的符号SiP.
(2)在这些元素中,Na(用元素符号填写,下同)是最活泼的金属元素;F是最活泼的非金属元素.
(3)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;NaOH碱性最强;能形成两性氢氧化物的元素是Al.
(4)写出①的最高价氧化物的化学式CO2
(5)比较⑤与⑥的化学性质,Na更活泼.
| 周期/族 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | ○ |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(2)在这些元素中,Na(用元素符号填写,下同)是最活泼的金属元素;F是最活泼的非金属元素.
(3)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;NaOH碱性最强;能形成两性氢氧化物的元素是Al.
(4)写出①的最高价氧化物的化学式CO2
(5)比较⑤与⑥的化学性质,Na更活泼.