题目内容
下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | SO2通入溴水中 | 溶液褪色 | SO2有漂白性 |
| B | 将Fe(NO3)2样品溶于稀H2SO4,滴加KSCN溶液 | 溶液变红 | Fe(NO3)2样品已氧化变质 |
| C | 将新制氯水和KI溶液在试管中混合后,加入CCl4,振荡静置 | 溶液分层,下层呈紫色 | 氧化性:Cl2>I2 |
| D | 分别向0.1 mol?L-1醋酸和饱和硼酸溶液中滴加0.1mol?L-1Na2CO3溶液 | 醋酸中有气泡产生,硼酸中没有气泡产生 | 酸性:醋酸>碳酸>硼酸 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价,氧化性、还原性强弱的比较,二氧化硫的化学性质
专题:
分析:A.二氧化硫和溴水发生氧化还原反应;
B.硝酸根离子在酸性条件下可氧化亚铁离子;
C.下层呈紫色,说明生成碘;
D.醋酸中有气泡产生,硼酸中没有气泡产生,说明醋酸可生成碳酸,酸性比碳酸强.
B.硝酸根离子在酸性条件下可氧化亚铁离子;
C.下层呈紫色,说明生成碘;
D.醋酸中有气泡产生,硼酸中没有气泡产生,说明醋酸可生成碳酸,酸性比碳酸强.
解答:
解:.二氧化硫和溴水发生氧化还原反应,说明二氧化硫具有还原性,故A错误;
B.硝酸根离子在酸性条件下可氧化亚铁离子,不能酸化,应直接加入KSCN,故B错误;
C.下层呈紫色,说明生成碘,可说明氧化性:Cl2>I2,氯气置换出碘,故C正确;
D.醋酸中有气泡产生,硼酸中没有气泡产生,说明醋酸可生成碳酸,酸性比碳酸强,可说明酸性:醋酸>碳酸>硼酸,故D正确.
故选CD.
B.硝酸根离子在酸性条件下可氧化亚铁离子,不能酸化,应直接加入KSCN,故B错误;
C.下层呈紫色,说明生成碘,可说明氧化性:Cl2>I2,氯气置换出碘,故C正确;
D.醋酸中有气泡产生,硼酸中没有气泡产生,说明醋酸可生成碳酸,酸性比碳酸强,可说明酸性:醋酸>碳酸>硼酸,故D正确.
故选CD.
点评:本题考查较为综合,涉及硝酸、二氧化硫以及氧化性、酸性的比较,为高考常见题型和高频考点,侧重于学生的分析能力和评价能力的考查,学习中注意相关基础知识的积累,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
工业上以铬铁矿(主要成分为FeO?Cr2O3)、碳酸钠、氧气、和硫酸为原料生产重铬酸钠(Na2Cr2O7?2H2O),其主要反应为:下列说法正确的是( )
(1)4FeO?Cr2O3+8Na2CO3+7O2
8Na2CrO4+2Fe2O3+8CO2
(2)2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2O.
(1)4FeO?Cr2O3+8Na2CO3+7O2
| ||
(2)2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2O.
| A、反应(1)和(2)均为氧化还原反应 |
| B、反应(1)的氧化剂是O2,还原剂是FeO?Cr2O3 |
| C、高温下,O2的氧化性强于Fe2O3,弱于Na2CrO4 |
| D、反应(1)中每生成1molNa2CrO4时电子转移3mol |
 如图所示的 甲、乙、丙三种物质,含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
如图所示的 甲、乙、丙三种物质,含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )①C ②H2O2 ③Na ④Fe ⑤HNO3.
| A、①③④ | B、①②⑤ |
| C、①②③⑤ | D、①②③④⑤ |
下列解释事实的方程式错误的是( )
| A、测得0.1 mol?L-1氨水的pH为11:NH3?H2O?NH4++OH- | ||||
| B、将Na块投入水中,产生气体:2Na+2H2O═2NaOH+H2↑ | ||||
C、用CuCl2溶液做导电实验,灯泡发光:CuCl2
| ||||
D、将1 mol?L-1FeCl3溶液滴入沸水中,得到透明红褐色液体:FeCl3+3H2O
|
用惰性电极电解下列物质的水溶液,一段时间后(温度不变),再加入一定质量的另一种物质(括号内物质),溶液能恢复到与电解前的溶液完全一样的是( )
| A、CuCl2(CuO) |
| B、NaOH(Na2O) |
| C、NaCl(NaCl) |
| D、H2SO4(H2O) |
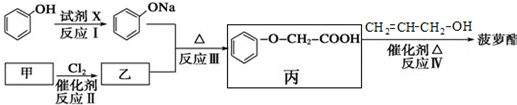
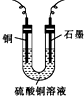 当pH为4~5时,Cu2+几乎不水解,而Fe3+几乎完全沉淀.某同学欲用电解纯净CuSO4溶液的方法来测定铜的相对原子质量.实验过程中使用肼(N2H4)-空气燃料电池作直流电源,其实验过程如图所示:
当pH为4~5时,Cu2+几乎不水解,而Fe3+几乎完全沉淀.某同学欲用电解纯净CuSO4溶液的方法来测定铜的相对原子质量.实验过程中使用肼(N2H4)-空气燃料电池作直流电源,其实验过程如图所示: