题目内容
20.下列实验操作中,错误的是( )| A. | 配制5%的食盐溶液时,将称量的食盐放在烧杯中加适量的蒸馏水搅拌溶解 | |
| B. | 用酸式滴定管准确量取10.00 mL KMnO4溶液 | |
| C. | 用500 mL容量瓶配制1 mol/L的NaOH溶液 | |
| D. | 用pH试纸测得新制氯水的pH为2 |
分析 A.配制5%的食盐溶液,根据称量的食盐质量计算溶液的质量,进而计算需要水的质量,将称量的食盐放在烧杯中加适量的蒸馏水搅拌溶解即可;
B.滴定管的精度为0.01mL,高锰酸钾具有强氧化性,可以腐蚀橡皮管,故应用酸式滴定管量取;
C.将20.0g氢氧化钠溶解后,冷却后转移到500mL容量瓶定容,所得溶液的浓度为1mol/L;
D.氯水有强氧化性,具有漂白性.
解答 解:A.配制5%的食盐溶液,根据称量的食盐质量计算溶液的质量,进而计算需要水的质量,将称量的食盐放在烧杯中加适量的蒸馏水搅拌溶解即可,故A正确;
B.高锰酸钾具有强氧化性,可以腐蚀橡皮管,故应用酸式滴定管量取,滴定管的精度为0.01mL,可以准确量取10.00mL溶液,故B正确;
C.将20.0g氢氧化钠溶解,冷却后转移到500mL容量瓶定容,所得溶液的浓度为1mol/L,故C正确;
D.氯水有强氧化性,具有漂白性,将新制氯水滴在pH试纸上先变红,红色立即褪去,故不能测定新制氯水的pH值,故D错误;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及溶液配制原理及实验基本操作、滴定管的使用、氯水的性质等,难度中等,D选项为易错点,容易忽略氯水的漂白性.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
14.下列分子中含有两个π键的是( )
| A. | O2 | B. | N2 | C. | H2O | D. | NH3 |
11.下列电离或水解方程式书写不正确的是( )
| A. | 碳酸氢钠的电离方程式为:NaHCO3═Na++HCO3- HCO3-?H++CO32- | |
| B. | 偏铝酸钠的水解方程式为:AlO2-+2H2O═Al(OH)3↓+OH- | |
| C. | 硫化铝溶于水的水解方程式为:Al2S3+6H2O═2Al(OH)3↓+3H2S↑ | |
| D. | 醋酸铵的水解方程式为:CH3COO-+NH4++H2O?CH3COOH+NH3•H2O |
8.在刚刚过去的一年中,发生了许多与化学相关的大事件.下列说法正确的是( )

| A. | 被称为“史上最严”的新《环境保护法》正式实施,我们要运用化学原理从源头上减少和消除工业生产对环境的污染 | |
| B. | 天津港爆炸事故救援过程中,消防员若发现存放金属钠、电石、甲苯二异氰酸酯等化学品的仓库起火,应立即用泡沫灭火器将火扑灭 | |
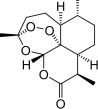
| C. | 世界卫生组织认为青蒿素(结构如图所示)联合疗法是当下治疗疟疾最有效的手段,烃类物质青蒿素已经拯救了上百万生命 | |
| D. | 某品牌化妆品在广告中反复强调产品中不含任何化学成分,是“十年专注自然护肤”的优质产品 |
15.下列有关事实的叙述正确的是( )
| A. | 电解饱和NaOH溶液时溶液的pH变大 | |
| B. | 在镀件上电镀铜时,可以不用金属铜做阳极,只要溶液中存在Cu2+就可以 | |
| C. | 电解稀硫酸制O2、H2时,铜做阳极 | |
| D. | 铝-空气燃料电池通常以NaOH溶液为电解液,电池在工作过程中电解液的pH保持不变 |
9.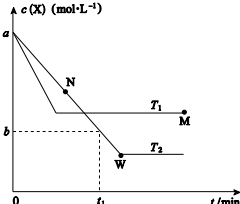 在恒容密闭容器中通入X 并发生反应:2X(g)?Y(g),温度T1、T2下X 的物质的量浓度c(X)随时间t 变化的曲线如图所示,下列叙述正确的是 ( )
在恒容密闭容器中通入X 并发生反应:2X(g)?Y(g),温度T1、T2下X 的物质的量浓度c(X)随时间t 变化的曲线如图所示,下列叙述正确的是 ( )
 在恒容密闭容器中通入X 并发生反应:2X(g)?Y(g),温度T1、T2下X 的物质的量浓度c(X)随时间t 变化的曲线如图所示,下列叙述正确的是 ( )
在恒容密闭容器中通入X 并发生反应:2X(g)?Y(g),温度T1、T2下X 的物质的量浓度c(X)随时间t 变化的曲线如图所示,下列叙述正确的是 ( )| A. | 该反应进行到M 点放出的热量大于进行到W 点放出的热量 | |
| B. | T2 下,在0~t1 时间内,v(Y)═$\frac{a-b}{{t}_{1}}$mol•L-1•min-1 | |
| C. | M 点的平衡常数小于W 点的平衡常数 | |
| D. | M 点时再加入一定量X,平衡后X 的转化率减小 |
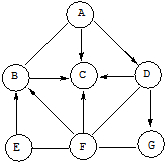 则原混合物中E、G的物质的量之比为1:1.
则原混合物中E、G的物质的量之比为1:1.