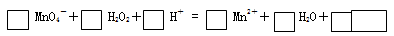题目内容
(13分)【化学—物质结构与性质】
科技日报报道:辉钼(MoS2)在纳米电子设备制造领域比硅或富勒烯(如C60)更有优势。从不同角度观察MoS2的晶体结构见图。已知:Mo位于第五周期VIB族。

(1)晶体硅中硅原子的轨道杂化类型为______。
(2)电负性:C______S(填“>”或“<”)。
(3)晶体硅和C60比较,熔点较高的是______。
(4)Mo元素基态原子的价电子排布式为____________。
(5)根据MoS2的晶体结构回答:
①每个Mo原子周围距离最近的S原子数目为______。
②Mo-S之间的化学键为______(填序号)。
A极性键 B非极性键 C配位键 D金属键 E范德华力
③MoS2纳米粒子具有优异的润滑性能,其原因是______。
31.(1)sp3(1分) (2)< (2分) (3)晶体硅(2分) (4)4d45s1(2分)
(5)①6(2分) ②AC(2分) ③MoS2具有层状结构,Mo与S同层间以共价键结合,层与层之间通过范德华力结合,外力作用层与层易发生相对滑动(2分)
【解析】
试题分析:(1)晶体硅中以正四面体结构为单元,说明硅原子采取sp3杂化方式;(2)最高价氧化物对应水化物酸性:H2CO3<H2SO4,则非金属性:C<S,所以电负性:C<S;(3)晶体硅是原子晶体,C60是分子晶体,则熔点:晶体硅>C60;(4)Mo位于第五周期VIB族,由能量最低原理、洪特规则可知,基态Mo原子的价电子排布式为4d45s1;(5)①读图可知,每个Mo原子周围距离最近的S由6个;②Mo-S之间的化学键为极性键和配位键,AC正确;③MoS2具有层状结构,Mo与S同层间以共价键结合,层与层之间通过范德华力结合,外力作用层与层易发生相对滑动。
考点:考查原子轨道杂化方式、电负性、熔点高低比较、价电子排布式、晶体结构、化学键、物质结构与性质等知识。

(12分)如下表所示为自然界中的多种铜矿石的主要成分:
矿石名称 | 黄铜矿 | 斑铜矿 | 辉铜矿 | 孔雀石 |
主要成分 | CuFeS2 | Cu5FeS4 | Cu2S | CuCO3·Cu(OH)2 |
请回答:
(1)上表所列铜化合物中,铜的质量百分含量最高的是 (填化学式);
(2)工业上以黄铜矿为原料。采用火法溶炼工艺生产铜。该工艺的中间过程包含反应:
2Cu2O+Cu2S 6Cu+SO2↑,则该反应的氧化剂与还原剂的物质的量之比是 ;
6Cu+SO2↑,则该反应的氧化剂与还原剂的物质的量之比是 ;
(3)火法溶炼工艺生产铜的尾气直接排放到大气中造成环境污染的后果是 ;处理该尾气可得到有价值的化学品,写出其中一种酸和一种盐的名称或化学式 、 。
(4)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是 (填字母)。
选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
A | 铜绿的主成分是碱式碱酸铜 | 可用稀盐酸除铜器表面的铜绿 | Ⅰ对;Ⅱ对;有 |
B | 铜表易形成致密的氧化膜 | 铜容器可以盛放浓硫酸 | Ⅰ对;Ⅱ对;有 |
C | 铁比铜活泼 | 铆在铜板上的铁钉在潮湿空气中不易生锈 | Ⅰ对;Ⅱ对;有 |
D | 蓝色硫酸铜晶体受热转化为白色硫酸铜粉末是物理变化 | 硫酸铜溶液可用作游泳池的消毒剂 | Ⅰ错;Ⅱ对;无 |
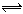 2C+2D,在4种不同情况下的反应速率分别为单位mol·Lˉ1·sˉ1:
2C+2D,在4种不同情况下的反应速率分别为单位mol·Lˉ1·sˉ1: ??H++A-,回答下列问题:
??H++A-,回答下列问题: 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示: