题目内容
3.判断下列各组离子能否大量共存①Ca2+ Na+ CO32- NO3-
②Ca2+ Na+ SO42- NO3-
③H+ K+ Cl- OH-
④NH4+ K+ OH- SO42-
⑤H+ K+ CO32- SO42-
⑥Na+ K+ CO32- OH-.
分析 ①钙离子与碳酸根离子反应生成碳酸钙沉淀;
②钙离子与硫酸根离子反应生成硫酸钙;
③氢离子与氢氧根离子反应;
④铵根离子与氢氧根离子反应;
⑤氢离子与碳酸根离子反应;
⑥四种离子之间不反应,能够共存.
解答 解:①Ca2+、CO32-之间反应生成碳酸钙沉淀,在溶液中不能大量共存;
②Ca2+、SO42-之间反应生成硫酸钙,在溶液中不能大量共存;
③H+、OH- 之间发生反应,在溶液中不能大量共存;
④NH4+、OH-之间发生反应,在溶液中不能大量共存;
⑤H+、CO32-之间发生反应,在溶液中不能大量共存;
⑥Na+、K+、CO32-、OH-之间不反应,在溶液中能够大量共存;
根据分析可知,①②③④⑤不能大量共存,⑥可以大量共存,
故答案为:①②③④⑤不能大量共存,⑥可以大量共存.
点评 本题考查离子共存的正误判断,为高考的高频题,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;试题侧重对学生基础知识的训练和检验,有利于培养学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
19.下列有关物质转化关系的说法中不正确的是( )
| A. | 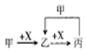 图中甲可能是Cl2,X可能是Fe | |
| B. |  图中反应一定是置换反应或复分解反应 | |
| C. | 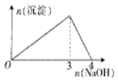 图中是向某溶液中滴加NaOH溶液的变化图象,原溶质可能是Al2(SO4)3 | |
| D. | 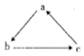 图中a可能为NaOH,b可能为Na2CO3,c可能为NaHCO3 |
20.下列关于有机化合物的说法正确的是( )
| A. | 乙醇室温下在水中的溶解度小于溴苯 | |
| B. | 氨基酸和蛋白质遇硫酸铜溶液均会变性 | |
| C. | 石油裂化和油脂皂化均是由高分子物质生成小分子物质的过程 | |
| D. | 苯和氯乙烯均能发生加成反应 |
17.在透明的酸性溶液中能大量共存的离子组是( )
| A. | Ba2+、K+、OH-、NO3- | B. | NH4+、Cu2+、SO42-、Cl- | ||
| C. | Al3+、Fe2+、SO42-、NO3- | D. | Na+、Ca2+、Cl-、CO32- |
15.某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如表数据(盐酸的物质的量浓度相等),下列分析推理正确的是( )
| 50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V${\;}_{C{O}_{2}}$(标况) | 2.24L | 3.36L | 3.36L |
| A. | 盐酸的物质的量浓度为5.0mol•L-1 | |
| B. | 根据表中数据计算出混合物中NaHCO3的物质的量分数为45.7% | |
| C. | 9.2g混合物中NaHCO3和KHCO3分别为5.0g和4.2g | |
| D. | 15.7g混合物恰好与盐酸完全反应 |
12.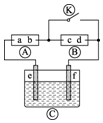 如图为直流电源,?为浸透饱和碘化钾溶液和淀粉溶液的滤纸,?为电镀槽.接通电路后发现?上的d点显蓝色.为实现铁上镀锌,接通
如图为直流电源,?为浸透饱和碘化钾溶液和淀粉溶液的滤纸,?为电镀槽.接通电路后发现?上的d点显蓝色.为实现铁上镀锌,接通 后,使c、d两点短路.下列叙述不正确的是( )
后,使c、d两点短路.下列叙述不正确的是( )
 如图为直流电源,?为浸透饱和碘化钾溶液和淀粉溶液的滤纸,?为电镀槽.接通电路后发现?上的d点显蓝色.为实现铁上镀锌,接通
如图为直流电源,?为浸透饱和碘化钾溶液和淀粉溶液的滤纸,?为电镀槽.接通电路后发现?上的d点显蓝色.为实现铁上镀锌,接通 后,使c、d两点短路.下列叙述不正确的是( )
后,使c、d两点短路.下列叙述不正确的是( )| A. | f电极为锌板 | B. | c极发生的反应为2H++2e-═H2↑ | ||
| C. | a为直流电源的正极 | D. | e极发生氧化反应 |
13.下列反应的离子方程式正确的是( )
| A. | 用氨水溶解氯化银沉淀:Ag++2NH3•H2O=[Ag(NH3)2]++2H2O | |
| B. | Mg(HCO3)2溶液中加入足量NaOH溶液:Mg2++2HCO3-+2OH-═Mg CO3↓+CO32-+2H2O | |
| C. | Na2O2固体投入H218O中:2H218O+2Na2O2=4Na++4OH-+18O2↑ | |
| D. | 苯酚钠溶液跟AlCl3溶液反应:3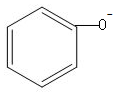 +Al3++3H2O→ +Al3++3H2O→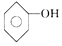 +Al(OH)3↓ +Al(OH)3↓ |

 ;⑧的原子结构示意图为
;⑧的原子结构示意图为 .
.