题目内容
15.下列有关晶体的说法中正确的是( )| A. | 氯化钾溶于水时离子键未被破坏 | B. | 分子间作用力越大,分子越稳定 | ||
| C. | 冰融化时分子中共价键发生断裂 | D. | 原子晶体中共价键越强,熔点越高 |
分析 A.氯化钾为离子晶体,溶于水电离;
B.分子的稳定性与共价键有关;
C.冰融化时只克服分子间作用力;
D.共价键越强,键能越大,则熔点越高.
解答 解:A.氯化钾为离子晶体,溶于水发生电离,离子键被破坏,故A错误;
B.分子间作用力影响物理性质,而分子的稳定性与共价键有关,故B错误;
C.水分子间存在氢键,属于分子间作用力,冰融化时只克服分子间作用力,共价键没有破坏,故C错误;
D.影响原子晶体熔沸点高低的因素为共价键,共价键越强,键能越大,则熔点越高,故D正确.
故选D.
点评 本题考查化学键类型和晶体类型的关系,为高频考点,侧重双基的考查,有利于培养学生良好的科学素养,提高学习的积极性,注意把握晶体类型的判断,把握共价键和氢键、分子间作用力的区别.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
5.下列说法中正确的是( )
| A. | 铵盐都易溶于水 | |
| B. | 铵盐受热分解都能得到氨气 | |
| C. | 除去NH4Cl溶液中少量的CaCl2,加过量的NH4HCO3溶液后过滤 | |
| D. | 铵盐与碱液共热都能生成使蓝色石蕊试变红的气体 |
6.关于如图所示装置的叙述,错误的是( )
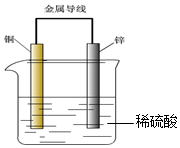

| A. | 锌是负极,随着放电的进行其质量逐渐减轻 | |
| B. | 放电过程中氢离子移向铜极,硫酸根离子移向锌极 | |
| C. | 电流从锌极经导线流向铜极 | |
| D. | 锌极上发生的是氧化反应,铜极上发生的是还原反应 |
3.下列有关说法错误的是( )
| A. | 磷原子的质子数为14 | B. | 氧元素在第二周期 | ||
| C. | 氯元素的最高化合价为+7 | D. | 还原性 Na<K |
10.将等物质的量的SO2和Cl2同时通入紫色石蕊试液中,可观察到的现象是( )
| A. | 先褪色,后复原 | B. | 立即褪色 | C. | 仍为紫色 | D. | 溶液变红色 |
7.下列叙述中,不正确的是( )
| A. | 天然气和沼气的主要成分是甲烷 | |
| B. | 乙醛含有碳氧双键,能发生加成反应 | |
| C. | 只有碳、氢两种元素组成的有机化合物称为烃 | |
| D. | 苯可以发生加成反应,因为苯中含有碳碳双键 |
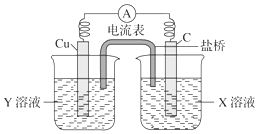 (1)利用反应Cu+2FeCl3═CuCl2+2FeCl2设计成如图所示的原电池,回答下列问题:
(1)利用反应Cu+2FeCl3═CuCl2+2FeCl2设计成如图所示的原电池,回答下列问题: