题目内容
3.要证明CuSO4溶液显蓝色不是由于SO42-造成的,下列实验无意义的是( )| A. | 观察K2SO4溶液的颜色 | |
| B. | 加水稀释CuSO4溶液,溶液颜色变浅 | |
| C. | 向CuSO4溶液中滴加过量NaOH溶液,振荡后静置,溶液变成无色 | |
| D. | 向CuSO4溶液中滴加过量Ba(NO3)2溶液,振荡后静置,溶液未变成无色 |
分析 CuSO4溶液中含有Cu2+、SO42-、H2O,要证明CuSO4溶液显蓝色不是由于SO42-离子造成的,只要排除SO42-、H2O的干扰,并用含有Cu2+的其它盐溶液对比判断.
解答 解:A.K2SO4溶液中含有SO42-不含Cu2+、K2SO4溶液呈无色,说明硫酸铜溶液呈蓝色不是SO42-离子造成,故A不选;
B.加水稀释后CuSO4溶液颜色变浅,溶液中仍然存在Cu2+、SO42-、H2O,无法确定哪种粒子造成的,故B选;
C.CuSO4+2NaOH=Na2SO4+Cu(OH)2↓,反应后溶液中SO42-仍然存在,但溶液颜色消失,说明硫酸铜溶液呈蓝色不是SO42-离子造成,故C不选;
D.CuSO4+Ba(NO3)2=BaSO4↓+Cu(NO3)2,振荡后静置,溶液颜色未消失,说明酸铜溶液呈蓝色不是SO42-离子造成,是Cu2+造成的,故D不选;
故选B.
点评 本题考查性质实验方案设计,根据物质的性质选取合适的试剂设计实验,有时要设计对比实验进行分析,题目难度中等.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案
相关题目
14. 一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
 一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )| A. | NaCl是非电解质 | |
| B. | NaCl溶液是电解质 | |
| C. | NaCl在水溶液中电离出了可以自由移动的离子 | |
| D. | 固体NaCl中没有离子 |
11.下列图示与对应的叙述相符合的是( )
| A. | 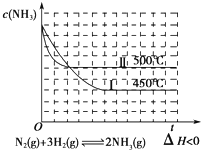 | B. | 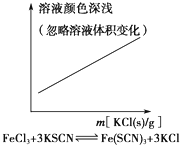 | ||
| C. | 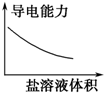 向稀醋酸中加入醋酸钠溶液 | D. | 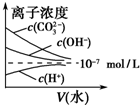 稀释苏打溶液 |
18.NA表示阿伏伽德罗常数.下列叙述中正确的是( )
| A. | 标准状况下,22.4 L水中含有的水分子数为NA | |
| B. | 4.0 g NaOH固体溶于100 mL水中,得到1 mol/L的 NaOH溶液 | |
| C. | 常温、常压下,22 g CO2中含有的氧原子数为NA | |
| D. | 0.5 mol/L Na2SO4溶液中,含有的离子总数为1.5NA |
8.设NA为阿伏伽德罗常数,根据Cu+4NNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,则下列叙述正确的是( )
| A. | 22.4LNO2含电子总数为23NA | |
| B. | 3.6gH2O中含有共价键的总数为0.2NA | |
| C. | 若生成的硝酸铜浓度为2mol/L,则1L该溶液中含有的Cu2+数为2N | |
| D. | 若有2molCu参与反应,则有4molHNO3被还原 |
15.下列说法正确的是( )
| A. | 高纯硅广泛用于制作光导纤维 | |
| B. | 将SO2通入到BaCl2溶液中可生成白色沉淀 | |
| C. | 向AlCl3溶液中滴加氨水,产生白色沉淀,再加过量的NaHSO4溶液,沉淀消失 | |
| D. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
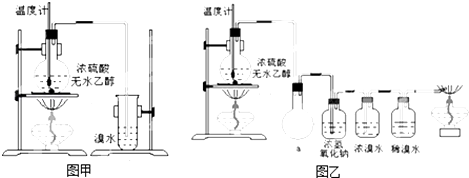
 CH2=CH2↑+H2O、CH2=CH2+Br2→CH2BrCH2Br.
CH2=CH2↑+H2O、CH2=CH2+Br2→CH2BrCH2Br.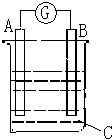 请根据如图所示回答:甲装置是由铜、锌和硫酸铜组成的原电池,
请根据如图所示回答:甲装置是由铜、锌和硫酸铜组成的原电池,