题目内容
体积相同的盐酸和醋酸两种溶液,n(Cl-)=n(CH3COO-)=0.01mol,下列叙述不正确的是( )
| A、它们与NaOH完全中和时,醋酸溶液所消耗的NaOH多 |
| B、两种溶液的物质的量浓度不相同 |
| C、分别用水稀释相同倍数时,n(Cl-)<n(CH3COO-) |
| D、它们分别与足量CaCO3反应时,放出的CO2一样多 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:n(Cl-)=n(CH3COO-)=0.01mol,溶液中氢离子浓度相等,醋酸是弱酸,部分电离,醋酸的物质的量难度一定大于盐酸的浓度
A、醋酸的浓度大于盐酸的浓度,等体积条件下醋酸的物质的量大;
B、醋酸的浓度大于盐酸的浓度;
C、稀释促进醋酸的电离;
D、醋酸的浓度大于盐酸的浓度,足量CaCO3反应时,醋酸生成的二氧化碳多.
A、醋酸的浓度大于盐酸的浓度,等体积条件下醋酸的物质的量大;
B、醋酸的浓度大于盐酸的浓度;
C、稀释促进醋酸的电离;
D、醋酸的浓度大于盐酸的浓度,足量CaCO3反应时,醋酸生成的二氧化碳多.
解答:
解:根据题中信息可知:n(Cl-)=n(CH3COO-)=0.01mol,溶液中氢离子浓度相等,醋酸是弱酸,部分电离,醋酸的物质的量浓度一定大于盐酸的浓度
A、它们与NaOH完全中和时,醋酸的物质的量多,醋酸溶液所消耗的NaOH多,故A正确;
B、醋酸是弱酸,部分电离,醋酸的物质的量浓度一定大于盐酸的浓度,所以两种溶液的物质的量浓度不相同,故B正确;
C、醋酸是弱电解质,部分电离,稀释后电离程度变大,醋酸根离子物质的量增大,所以分别用水稀释相同倍数时,n(Cl-)<n(CH3COO-),故C正确;
D、醋酸的浓度大于盐酸的浓度,足量CaCO3反应时,醋酸生成的二氧化碳多,故D错误;
故选:D.
A、它们与NaOH完全中和时,醋酸的物质的量多,醋酸溶液所消耗的NaOH多,故A正确;
B、醋酸是弱酸,部分电离,醋酸的物质的量浓度一定大于盐酸的浓度,所以两种溶液的物质的量浓度不相同,故B正确;
C、醋酸是弱电解质,部分电离,稀释后电离程度变大,醋酸根离子物质的量增大,所以分别用水稀释相同倍数时,n(Cl-)<n(CH3COO-),故C正确;
D、醋酸的浓度大于盐酸的浓度,足量CaCO3反应时,醋酸生成的二氧化碳多,故D错误;
故选:D.
点评:本题考查了醋酸在溶液中的电离,以及加水稀释对醋酸电离平衡的影响,注重基础知识的考查,本题难度不大.

练习册系列答案
相关题目
除去氯气中混有的少量的氯化氢气体,最好选用( )
| A、水 | B、饱和食盐水 |
| C、纯碱溶液 | D、烧碱溶液 |
将一定量的锌与100mL 18.5mol/L H2SO4充分反应后,锌完全溶解,同时生成气体A 22.4L(标准状况).将反应后的溶液稀释至1L,测得溶液的pH=1,则下列叙述中错误的是( )
| A、气体A为SO2和H2的混合物 |
| B、反应中共消耗Zn 65g |
| C、气体A中SO2和H2的体积比为1:4 |
| D、反应中共转移电子2mol |
下列各组物质性质的比较,正确的是( )
| A、酸性:HClO4>H3PO4>H2SO4 |
| B、碱性:KOH>NaOH>Mg(OH)2 |
| C、离子半径:O2->F->Cl->Na+ |
| D、氢化物稳定性:H2S>HF>H2O |
将15.3克的Mg和Cu混合物完全溶解与足量的硝酸中收集反应产生的X气体.在向所得的溶液中加入过量的NaOH产生25.5克沉淀,则气体X的成分可能是( )
| A、0.6molNO |
| B、0.3molNO2和0.3molNO |
| C、0.2molNO2和0.1molN2O4 |
| D、0.1molNO和0.2molNO2和0.05molN2O4 |
下列实验操作中,错误的是( )
| A、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B、把几滴FeCl3饱和溶液滴入25mL沸水中制备Fe(OH)3胶体 |
| C、过滤可以除掉粗盐中可溶于水的杂质 |
| D、碘易溶于有机溶剂,可用CCl4萃取碘水中的碘 |
下列反应属于加成反应的是( )
A、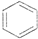 +HNO3 +HNO3
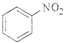 +H2O +H2O | |||
B、CH2=CH2+Br2→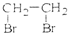 | |||
C、CH3CH2OH+CH3COOH
| |||
D、CH4+Cl2
|