题目内容
16.下列物质属于正盐的是( )| A. | NaOH | B. | NaNO3 | C. | KHSO4 | D. | HCl |
分析 酸碱恰好完全反应生成的盐为正盐,正盐由金属阳离子(或铵根离子)与酸根离子构成,以此来解答.
解答 解:A.NaOH为碱,在水中电离的阴离子全部为氢氧根离子,故A不选;
B.NaNO3由钠离子与硝酸根离子构成,属于盐,故B选;
C.KHSO4为酸式盐,为硫酸中氢离子被KOH部分中和的产物,故C不选;
D.HCl为酸,在水中电离的阳离子全部为氢离子,故D不选;
故选B.
点评 本题考查物质的分类,为高频考点,把握酸碱盐的构成为解答的关键,侧重分析与应用能力的考查,注意酸式盐与正盐的区别,题目难度不大.

练习册系列答案
相关题目
11. 铁有δ、γ、α三种晶体结构,以下依次是δ、γ、α三种晶体不同温度下转化的图示,下列有关说法不正确的是( )
铁有δ、γ、α三种晶体结构,以下依次是δ、γ、α三种晶体不同温度下转化的图示,下列有关说法不正确的是( )
 铁有δ、γ、α三种晶体结构,以下依次是δ、γ、α三种晶体不同温度下转化的图示,下列有关说法不正确的是( )
铁有δ、γ、α三种晶体结构,以下依次是δ、γ、α三种晶体不同温度下转化的图示,下列有关说法不正确的是( )| A. | δ-Fe晶体中与相邻铁原子距离相等且最近的铁原子有8个 | |
| B. | γ-Fe晶体中与相邻铁原子距离相等且最近的铁原子有12个 | |
| C. | α-Fe晶胞边长若为a cm,y-Fe晶胞边长若为b cm,则a-Fe和y-Fe两种晶体的 密度比为b3:a3 | |
| D. | 将铁加热到1500℃后分别急速冷却和缓慢冷却,得到的晶体类型不同 |
1.下列说法不正确的是( )
| A. | 在配制一定物质的量浓度溶液的定容步骤时,俯视凹液面,所配溶液浓度偏高 | |
| B. | 向盛有5mL 4%和5mL 12%的过氧化氢溶液中分别加入几滴等浓度的氯化铁溶液,后者产生气泡速率快 | |
| C. | KI溶液中加少量新制的氯水,再加少量苯充分振荡后静置,上层为紫红色 | |
| D. | 用pH试纸测溶液的pH和用红色石蕊试纸检测气体时均不需要润湿 |
5.氯气是一种重要的工业原料.工业上利用反应3Cl2+2NH3═N2+6HCl检查氯气管道是否漏气.下列说法错误的是(注意:HCl与NH3极易反应而生成白烟)( )
| A. | 若管道漏气遇氨就会产生白烟 | B. | 该反应利用了Cl2的强氧化性 | ||
| C. | 生成1molN2有6mol电子转移 | D. | 该反应属于复分解反应 |


 +2nH2O⑩
+2nH2O⑩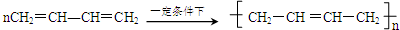
 如图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态).由图可知Mg与卤素单质的反应均为放热(填“放热”或“吸热”)反应.
如图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态).由图可知Mg与卤素单质的反应均为放热(填“放热”或“吸热”)反应.