题目内容
下列离子可以在同一溶液中大量共存的是( )
| A、Fe3+、H+、SO42-、NO3- |
| B、H+、Ba2+、NO3-、SO42- |
| C、Al3+、H+、CO32-、AlO2- |
| D、Fe3+、Mg2+、SCN-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:根据离子之间不能结合生成沉淀、气体、水等,不能相互促进水解,不能发生络合反应等,则离子大量共存,以此来解答.
解答:
解:A.该组离子之间不反应,可大量共存,故A正确;
B.Ba2+、SO42-结合生成沉淀,不能大量共存,故B错误;
C.H+分别与CO32-、AlO2-反应,Al3+分别与CO32-、AlO2-相互促进水解,不能大量共存,故C错误;
D.Fe3+、SCN-结合生成络离子,不能大量共存,故D错误;
故选A.
B.Ba2+、SO42-结合生成沉淀,不能大量共存,故B错误;
C.H+分别与CO32-、AlO2-反应,Al3+分别与CO32-、AlO2-相互促进水解,不能大量共存,故C错误;
D.Fe3+、SCN-结合生成络离子,不能大量共存,故D错误;
故选A.
点评:本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应、水解反应、络合反应的离子共存考查,综合性较强,题目难度不大.

练习册系列答案
相关题目
醋酸溶液中存在电离平衡CH3COOH?H++CH3COO-,下列叙述不正确的是( )
| A、醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-) |
| B、0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)增大 |
| C、CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动 |
| D、pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH>7 |
现有①MgSO4,②Ba(NO3)2,③NaOH,④CuCl2,⑤KCl五种溶液,不加任何其他试剂,被鉴别出的先后顺序正确的是( )
| A、④③①②⑤ |
| B、④⑤③②① |
| C、④③②①⑤ |
| D、④②③①⑤ |
已知2mol氢气燃烧生成水蒸气时,放出484kJ热量.下列热化学方程式正确的是( )
| A、2H2(g)+O2(g)=2H2O(g)△H=+484kJ?mol-1 | ||
| B、2H2(g)+O2(g)=2H2O(l)△H=-484kJ?mol-1 | ||
C、H2(g)+
| ||
D、H2(g)+
|
下列物质属于芳香烃,但不是苯的同系物的是( )
①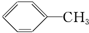 ②
②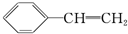 ③
③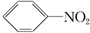 ④
④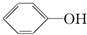 ⑤
⑤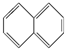 ⑥
⑥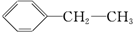
①
 ②
②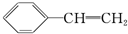 ③
③ ④
④ ⑤
⑤ ⑥
⑥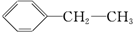
| A、③④ | B、②⑤ |
| C、①②⑤⑥ | D、②③④⑤⑥ |
 中和滴定:
中和滴定: