题目内容
14.现向含AgBr的饱和溶液中,加入固体AgNO3,则C(Br-)变小(填“变大”“变小”或“不变”)分析 AgBr饱和溶液中存在沉淀溶解平衡:AgBr(s)?Ag+(aq)+Br-(aq),加入AgNO3溶液后,溶液中银离子浓度增大,平衡向着逆向移动,据此判断溴离子浓度变化.
解答 解:在AgBr饱和溶液中存在沉淀溶解平衡:AgBr(s)?Ag+(aq)+Br-(aq),加入AgNO3溶液后,c(Ag+)增大,溶解平衡向着逆向移动,则溶液中c(Br-)变小,
故答案为:变小.
点评 本题考查了难溶电解质的沉淀溶解平衡及其影响,题目难度不大,注意掌握影响溶解平衡的因素,试题侧重基础知识的考查,培养了稀硝酸的灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.含有2~5个碳原子的直链烷烃沸点和燃烧热的数据见下表:( )
*燃烧热:1mol物质完全燃烧,生成二氧化碳、液态水时所放出的热量.根据表中数据,下列判断错误的是( )
| 烷烃名称 | 乙烷 | 丙烷 | 丁烷 | 戊烷 |
| 沸点(℃) | -88.6 | -42.1 | -0.5 | 36.1 |
| *燃烧热(kJ•mol-1) | 1560.7 | 2219.2 | 2877.6 | 3535.6 |
| A. | 正庚烷在常温常压下肯定不是气体 | |
| B. | 直链烷烃燃烧热和其所含碳原子数呈线性关系 | |
| C. | 随碳原子数增加,直链烷烃沸点逐渐升高 | |
| D. | 随碳原子数增加,直链烷烃沸点和燃烧热都成比例增加 |
2.在25.00ml碱式滴定管中盛有溶液,液面恰好在20.00ml刻度处,现将滴定管中全部溶液放出,流入量筒内,所得溶液体积为( )
| A. | 5mL | B. | 20mL | C. | 大于5mL | D. | 小于5mL |
9.在一定条件下,Na2CO3溶液存在水解平衡:CO32-+H2O?HCO3-+OH-,下列说法正确的是( )
| A. | 稀释溶液,水解平衡常数增大 | |
| B. | 升高温度,C(CO32-) 减小 | |
| C. | 稀释溶液,溶液中所有离子浓度均减小 | |
| D. | 加入NaOH(s),溶液pH减小 |
19.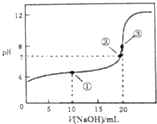 常温下,用0.1000mol•L-1NaOH溶液滴定20.00mL0.1000mol•L-1CH3COOH溶液所得曲线如图.下列说法正确的是( )
常温下,用0.1000mol•L-1NaOH溶液滴定20.00mL0.1000mol•L-1CH3COOH溶液所得曲线如图.下列说法正确的是( )
 常温下,用0.1000mol•L-1NaOH溶液滴定20.00mL0.1000mol•L-1CH3COOH溶液所得曲线如图.下列说法正确的是( )
常温下,用0.1000mol•L-1NaOH溶液滴定20.00mL0.1000mol•L-1CH3COOH溶液所得曲线如图.下列说法正确的是( )| A. | 滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) | |
| B. | ①处水的电离程度大于②处水的电离程度 | |
| C. | ②处加入的NaOH溶液恰好将CH3COOH中和 | |
| D. | ③处所示溶液:c(Na+)<c(CH3COO-) |
3.下列说法不正确的是( )
| A. | 粗铜电解精炼时,应将粗铜与直流电源的正极相连 | |
| B. | 金属的吸氧腐蚀的过程中,正极的电极反应式为O2+4e-+2H2O═4OH- | |
| C. | 燃料电池中加入燃料的电极一定是电池的负极 | |
| D. | 在生产生活中,为保护钢铁器件免受腐蚀,应将该器件与直流电源的正极相连 |