题目内容
13.金属铝在酸性或碱性溶液中均可与NO3-发生氧化还原反应,转化关系如下: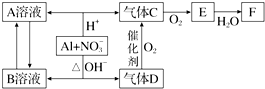
已知,气体D的大量生产曾经解决了地球上因粮食不足而导致的饥饿和死亡问题,气体D和F反应可生成盐.气体D和A溶液反应生成白色沉淀.气体C为无色气体,气体E为红棕色气体.B溶液加入过量的F溶液能生成A溶液.
请回答下列问题:
(1)C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C、E转化为无毒的气态单质,该单质为N2.
(2)完成并配平下列离子方程式:1Al+1NO3-+4H+→1Al3++1NO↑+2H2O.
(3)D→C反应的化学方程式是4NH3+5O2$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O.
(4)除去气体C中的杂质气体E的化学方法:3NO2+H2O═2HNO3+NO(用化学方程式表示).
分析 金属铝在酸性或碱性溶液中均可与NO3-发生氧化还原反应,由转化关系图可知,在酸性环境下,反应生成铝盐和一氧化氮,碱性环境下生成偏铝酸盐和氨气,氨气催化氧化可以生成一氧化氮和水,一氧化氮可以和氧气反应生成二氧化氮,故A为硝酸铝,B为偏铝酸盐,C为NO,D为氨气,E为二氧化氮,F为硝酸,然后结合元素化合物性质及化学用语来解答.
解答 解:金属铝在酸性或碱性溶液中均可与NO3-发生氧化还原反应,由转化关系图可知,在酸性环境下,反应生成铝盐和一氧化氮,碱性环境下生成偏铝酸盐和氨气,氨气催化氧化可以生成一氧化氮和水,一氧化氮可以和氧气反应生成二氧化氮,故A为硝酸铝,B为偏铝酸盐,C为NO,D为氨气,E为二氧化氮,F为硝酸,
(1)氨气可以和一氧化氮或是二氧化氮发生氧化还原反应生成无毒气体单质为氮气,化学式为N2,故答案为:N2;
(2)酸性条件下,Al和硝酸根离子发生氧化还原反应生成铝离子和一氧化氮,转移电子数为3,配平方程式为1Al+1NO3-+4H+═1Al3++1NO↑+2H2O,故答案为:1Al+1NO3-+4H+═1Al3++1NO↑+2H2O;
(3)D→C是氨气发生催化氧化生成NO、水,反应的化学方程式:4NH3+5O2$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O,
故答案为:4NH3+5O2$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O;
(4)二氧化氮可以和水发生反应生成硝酸和一氧化氮,3NO2+H2O═2HNO3+NO,可以用水除去一氧化氮中的二氧化氮,故答案为:3NO2+H2O═2HNO3+NO.
点评 本题是一道有关元素以及化合物知识的框图推断题,考查学生分析和解决问题的能力,难度不大.

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案| A. | 6种 | B. | 10种 | C. | 11种 | D. | 12种 |
| A. | 因为SO2有漂白性,所以它能使品红溶液、溴水褪色 | |
| B. | SO2和Cl2都有漂白作用,将两种气体同时作用于湿润的有色布条,漂白效果更好 | |
| C. | 在有些反应中显示氧化性,在有些反应中显示还原性 | |
| D. | 将SO2气体通入装有FeCl3溶液的试管里,黄色逐渐褪去 |
| A. | 碳氢化合物的通式为CnH2n+2 | B. | 甲烷是一种比较洁净的能源 | ||
| C. | 石油的主要成分是碳氢化合物 | D. | 甲烷的二氯代物无同分异构体 |
| A. | 油脂水解可得到氨基酸和甘油 | |
| B. | 淀粉和纤维素水解最终产物都是葡萄糖 | |
| C. | 蛋白质水解的最终产物是氨基酸,某些蛋白质可用硝酸来检验 | |
| D. | 葡萄糖可用新制的氢氧化铜来检验 |
| A. | 需要加热才能进行的化学反应一定是吸热反应 | |
| B. | 放热反应不需要加热即可发生 | |
| C. | 放热反应常温下易发生 | |
| D. | 反应是放热还是吸热,要看反应物和生成物所具有的总能量的相对大小,不能看反应条件 |
| A. | 甲烷的电子式为: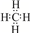 ,分子中各原子都达到“八电子”稳定结构 ,分子中各原子都达到“八电子”稳定结构 | |
| B. | CHCl3只有一种结构,说明甲烷是以碳原子为中心的正四面体结构 | |
| C. | CH4比SiH4分子稳定,说明碳元素比硅元素非金属性强 | |
| D. | CH3Cl的四个价键的长度和强度相同,夹角相等 |
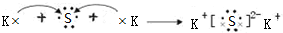 ,其化合物中化学键的类型是离子键.
,其化合物中化学键的类型是离子键.