题目内容
足量锌片和100mL5mol/L的稀H2SO4反应时,为减慢反应速率,又不影响生成氢气的总量,可采用的方法是( )
| A、加入几滴CuSO4溶液 |
| B、加入少量水 |
| C、升高温度 |
| D、加入少量Na2CO3 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:锌足量,则生成氢气由硫酸决定,为了减慢反应速率,且不影响生成氢气的总量,可减小氢离子的浓度,但不能改变硫酸的物质的量,以此来解答.
解答:
解:A.加入几滴CuSO4溶液,锌置换出铜,形成原电池反应,反应速率增大,故A错误;
B.加入少量水,硫酸浓度降低,反应速率减小,故B正确;
C.升高温度,反应速率增大,故C错误;
D.加入少量Na2CO3,消耗硫酸,溶液生成氢气的总量减小,故D错误.
故选B.
B.加入少量水,硫酸浓度降低,反应速率减小,故B正确;
C.升高温度,反应速率增大,故C错误;
D.加入少量Na2CO3,消耗硫酸,溶液生成氢气的总量减小,故D错误.
故选B.
点评:本题考查影响反应速率的因素,为高考常考考点,注意Zn过量,生成氢气由硫酸决定,把握浓度、温度、原电池对反应速率的影响即可解答,题目难度不大.

练习册系列答案
相关题目
下列有关化学用语正确的是( )
A、Cl-离子的结构示意图: |
| B、乙醇的分子式:CH3CH2OH |
C、丙烷分子的比例模型示意图: |
D、甲烷的结构式为: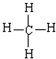 |
某溶液中含有NH
、Mg2+、Fe2+、Al3+和SO
五种离子,若向其中加入过量的Ba(OH)2溶液,微热并搅拌,再加入过量的氢碘酸,溶液中大量减少的离子有( )
+ 4 |
2- 4 |
| A、4种 | B、3种 | C、2种 | D、1种 |
下列离子方程式或化学反应方程式与所述事实相符且正确的是( )
| A、将2mol SO3气体通入一密闭容器中,反应达平衡后吸收Q kJ热量,则该反应的热化学方程式为:2SO3(g)?2SO2(g)+O2(g)△H=+Q kJ/mol |
| B、向20mL0.5mol?L-1 FeBr2(aq)中通入224mL Cl2(标准状况):2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
| C、以金属银为阳极电解饱和硫酸铜溶液 Cu2++2H2O=2Cu+O2↑+4H+ |
| D、NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
下列化学反应既是放热反应,同时又是氧化还原反应的是( )
| A、二氧化碳气体与碳单质高温下的反应 |
| B、八水合氢氧化钡固体与氯化铵固体的反应 |
| C、酸碱中和反应 |
| D、过氧化钠固体与二氧化碳气体的反应 |
根据下列原子结构示意图判断,化学性质最稳定的是( )
A、 |
B、 |
C、 |
D、 |
下列各反应的离子方程式中,错误的是( )
| A、铁片放入过量的稀硝酸中:3Fe+8H++2NO3-=3Fe2++2NO2↑+4H2O |
| B、硫酸铝溶液中加入过量的氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| C、将铝片放入过量NaOH溶液中:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
| D、偏铝酸钠与过量盐酸反应:AlO2-+4H+=Al3++2H2O |
提纯含有少量硝酸钡杂质的硝酸钾溶液,设计实验方案为
 则X试剂为( )
则X试剂为( )
 则X试剂为( )
则X试剂为( )| A、Na2CO3 |
| B、K2CO3 |
| C、Na2SO4 |
| D、K2SO4 |