题目内容
3.(1)实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是A.A.CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H<0
B.C(s)+H2O(g)=CO(g)+H2(g)△H>0
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H<0
(2)以KOH溶液为电解质溶液,依据(1)中所选反应设计一个原电池,其负极电池反应式为:CH4-8e-+10OH-=CO32-+7H2O;
(3)燃料电池是一种高效、环境友好的发电装置.燃料电池的能量转化率理论上可高达85%~90%(现在实际已达到40%~60%).CO、CH4、C2H5OH是常用的燃料,它们每1mol分别完全燃烧生成CO2(g)及H2O(l)时,放出的热量依次为283.0kJ、890.3kJ、1366.8kJ.相同质量的这3种燃料,完全燃烧时放出热量最多的是CH4(填写物质的化学式).
分析 (1)能设计成原电池的反应必须是放热反应,同时必须是氧化还原反应;
(2)燃料电池中,负极上投放燃料,正极上投放氧化剂,负极上燃料失电子发生氧化反应,正极上氧化剂得电子发生还原反应;
(3)根据CO、CH4、C2H5OH的相对分子质量分别为28、16、46和每1mol分别完全燃烧生成CO2(g)及H2O(l)时,放出的热量依次为283.0kJ、890.3kJ、1366.8kJ,计算1gCO、CH4、C2H5OH完全燃烧时,放出热量进行比较.
解答 解:(1)能设计成原电池的反应必须是放热反应,同时必须是氧化还原反应,
A.该反应是氧化还原反应且属于放热反应,故A正确;
B.该反应不是氧化还原反应,故B错误;
C.该反应不是氧化还原反应,故C错误;
故选:A;
(2)燃料电池中,负极上投放燃料,正极上投放氧化剂,负极上一氧化碳失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为CH4-8e-+10OH-=CO32-+7H2O;
故答案为:CO-2e-+4OH-=CO32-+2H2O;
(3)CO、CH4、C2H5OH的相对分子质量分别为28、16、46,又因为它们每1mol分别完全燃烧生成CO2(g)及H2O(l)时,放出的热量依次为283.0kJ、890.3kJ、1366.8kJ,所以1gCO、H2、CH4、C2H5OH完全燃烧时,放出热量分别为:$\frac{283}{28}$,$\frac{890.3}{16}$,$\frac{1366.8}{46}$,则相同质量的以上四种燃料,完全燃烧时放出热量最多的是CH4,故答案为:CH4.
点评 本题以原电池、电解池原理为载体考查了原电池的设计、金属的腐蚀与防护,注意能设计成原电池的反应必须是放热反应,同时必须是氧化还原反应.

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案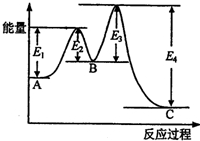 某反应由两步反应A?B?C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )
某反应由两步反应A?B?C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )| A. | 两步反应均为吸热反应 | B. | 稳定性C>A>B | ||
| C. | A与C的能量差为E4 | D. | A?C反应,反应条件一定要加热 |
| A. | 侯氏制碱法是先将CO2通入饱和NaCl溶液后,再通入NH3 | |
| B. | 新型材料聚酯纤维、光导纤维都属于有机高分子材料 | |
| C. | PM2.5是指大气中直径≤2.5×10-6m的颗粒物(气溶胶),可通过加水吸收后再利用过滤的方法分离PM2.5微粒和可溶性吸附物 | |
| D. | “神十”航天服是由碳化硅陶瓷和碳纤维复合而制成的,它是一种新型无机非金属材料 |
| A. | 0.168L | B. | 0.112L | C. | 0.672L | D. | 0.224L |
| A. | 1,2二氯丙烯 | B. | 2丁炔 | C. | 丙烯 | D. | 1丁烯 |
| A. | D>B>A>C>E | B. | D>A>B>C>E | C. | A>B>C>E>D | D. | D>E>B>A>C |
| A. | 电解池的反应属于自发过程 | |
| B. | 化学反应热效应数值与参加反应的物质多少有关 | |
| C. | 化学反应过程中的能量变化除了热能外,也可以是光能、电能等 | |
| D. | 热化学方程式中的化学计量数只表示物质的量,可以是分数 |
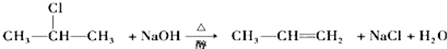
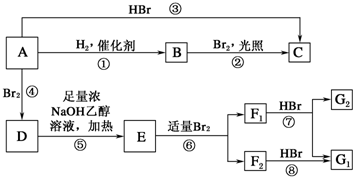
 ;A的结构简式为(CH3)2C═C(CH3)2;E的结构简式为
;A的结构简式为(CH3)2C═C(CH3)2;E的结构简式为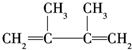 ;F1的结构简式为
;F1的结构简式为
 .
. .
.