题目内容
8.下列反应的离子方程式书写正确的是( )| A. | MgO溶于稀盐酸中:O2-+2H+═H2O | |
| B. | 碳酸钙中滴加稀盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | 实验室用MnO2反应制Cl2:MnO2+2H++2Cl-═Cl2↑+Mn2++H2O | |
| D. | 向氢氧化钠溶液中通入过量二氧化碳:OH-+CO2=HCO3- |
分析 A.氧化物应保留化学式;
B.碳酸钙为沉淀,应保留化学式;
C.原子个数不守恒;
D.二氧化碳过量,反应生成碳酸氢钠.
解答 解:A.MgO溶于稀盐酸中,离子方程式:MgO+2H+═H2O+Mg2+,故A错误;
B.碳酸钙中滴加稀盐酸,离子方程式:CaCO3+2H+═CO2↑+H2O+Ca2+,故B错误;
C.实验室用MnO2反应制Cl2,离子方程式:MnO2+4H++2Cl-═Cl2↑+Mn2++2H2O,故C错误;
D.向氢氧化钠溶液中通入过量二氧化碳,离子方程式:OH-+CO2=HCO3-,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写的方法是解题关键,注意化学式的拆分、原子个数守恒,题目难度不大.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
18.对下列各组离子共存问题的评价及离子方程式书写正确的是( )
| 选项 | 离子组 | 评 价 |
| A | H+、Fe2+、NO3-、Cl- | 不能大量共存于同一溶液中,因为发生了氧化还原反应: 4Fe2++2NO3-+6H+═4Fe3++2NO↑+3H2O |
| B | Na+、CO32-、Cl-、Al3+ | 不能大量共存于同一溶液中,因Al3+和CO32-都要发生水解且相互促进:2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑ |
| C | Fe3+、K+、SCN-、Br- | 不能大量共存于同一溶液中,因为有红色沉淀生成: Fe3++3SCN-═Fe(SCN)3↓ |
| D | HCO3-、OH-、Na+、Ca2+ | 不能大量共存于同一溶液中,因会发生如下反应: HCO3-+OH-═CO2↑+H2O |
| A. | A | B. | B | C. | C | D. | D |
19.下列有关实验的说法正确的是( )
| A. | 配制FeSO4溶液,应先将盐溶解在稀硫酸中,再加水稀释到所需浓度,并加入少量铁屑 | |
| B. | 切割白磷时,必须用镊子夹取,置于桌面上的玻璃片上,小心用刀切割 | |
| C. | 向淀粉溶液中加入稀硫酸,水浴加热一段时间.要证明淀粉已水解,取样后加入银氨溶液,水浴加热,观察是否有银镜生成 | |
| D. | 配制硫酸溶液时,可先在量筒内加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
3.为了提纯下列物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是( )
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 溴苯(溴) | 水 | 分液 |
| B | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| C | 苯(苯酚) | NaOH溶液 | 分液 |
| D | 甲烷(乙烯) | KMnO4酸性溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
13.在实验室,下列试剂不需保存在棕色试剂瓶内的是( )
| A. | 浓硝酸 | B. | 新制溴水 | C. | 浓盐酸 | D. | 硝酸银溶液 |
20.下列过程只需要克服分子间作用力的是( )
| A. | HCl气体溶于水 | B. | 碘单质升华 | ||
| C. | 氯化镁受热熔化 | D. | 二氧化硅受热熔化 |
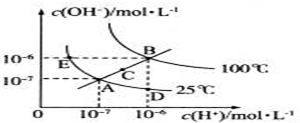
17.25℃时,水的电离达到平衡:H2O?H++OH--;△H>0,下列叙述正确的是( )
| A. | 向水中加入稀氨水,平衡逆向移动,c(OH-)降低 | |
| B. | 向水中加入少量固体NaHSO4,c(H+)增大,KW不变 | |
| C. | 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)减小 | |
| D. | 将水加热,KW增大,pH不变 |
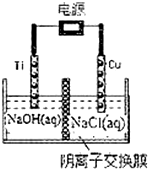 硝酸是一种重要的化工原料,工业上一般以氨气为原料来制备硝酸.请回答:
硝酸是一种重要的化工原料,工业上一般以氨气为原料来制备硝酸.请回答: