题目内容
(1)常温下,FeCl3溶液的pH 7(填“>”“<”或“=”),其原因是 (用离子方程式表示).
(2)向0.1mol?L-1 CH3COOH溶液中滴加NaOH溶液至溶液呈中性,则c(Na+) c(CH3COO-)(填“>”“<”或“=”).
(2)向0.1mol?L-1 CH3COOH溶液中滴加NaOH溶液至溶液呈中性,则c(Na+)
考点:盐类水解的应用
专题:盐类的水解专题
分析:(1)氯化铁为强酸弱碱盐,铁离子水解导致其溶液呈酸性;
(2)混合溶液呈中性,则c(H+)=c(OH-),再结合电荷守恒判断钠离子和醋酸根离子浓度相对大小.
(2)混合溶液呈中性,则c(H+)=c(OH-),再结合电荷守恒判断钠离子和醋酸根离子浓度相对大小.
解答:
解:(1)FeCl3为强酸弱碱盐,水解呈酸性,离子方程式为Fe3++3H2O?Fe(OH)3+3H+,其pH<7,故答案为:<;Fe3++3H2O?Fe(OH)3+3H+;
(2)混合溶液呈中性,则c(H+)=c(OH-),溶液中存在电荷守恒c(H+)+c(Na+)=c(CH3COO-)+c(OH-),所以c(Na+)=c(CH3COO-),故答案为:=.
(2)混合溶液呈中性,则c(H+)=c(OH-),溶液中存在电荷守恒c(H+)+c(Na+)=c(CH3COO-)+c(OH-),所以c(Na+)=c(CH3COO-),故答案为:=.
点评:本题考查了盐类水解、混合溶液中离子浓度大小判断,根据“谁强谁显性、谁弱谁水解”来确定氯化铁溶液的酸碱性,再结合电荷守恒判断酸碱混合溶液中离子浓度大小,题目难度不大.

练习册系列答案
 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
2010 年广州亚运会的良好环境给人们留下了深刻印象.下列措施不利于节能减排、改善环境的是( )
| A、贯彻“限塑令”、加快研发利用可降解塑料、 |
| B、加速建设地铁轨道交通、减少汽车尾气排放 |
| C、发展低碳经济、推广城市太阳能照明系统 |
| D、使用填埋法处理未经分类的生活垃圾 |
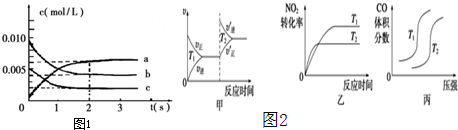 氮是大气中含量最多的气体,研究氮及其化合物对人类有重要的意义.
氮是大气中含量最多的气体,研究氮及其化合物对人类有重要的意义. 在一定条件下进行化学反应,请根据以下的转化关系回答下列问题,
在一定条件下进行化学反应,请根据以下的转化关系回答下列问题, 据测定,指示剂酚酞的结构简式可表示为则
据测定,指示剂酚酞的结构简式可表示为则