题目内容
4.表示阿伏加德罗常数,下列说法正确的是( )| A. | 0.5molAl与足量盐酸反应转移电子数为1NA | |
| B. | 标准状况下22.4LH2中含中子数为2 NA | |
| C. | 0.5mol CH4所含电子数为5 NA | |
| D. | 1L1 mol/L醋酸溶液中离子总数为2 NA |
分析 A、铝和盐酸反应后变为+3价;
B、氢气中不含中子;
C、甲烷为10电子分子;
D、醋酸为弱电解质,不能完全电离.
解答 解:A、铝和盐酸反应后变为+3价,故0.5mol铝反应后转移1.5NA个电子,故A错误;
B、氢气中不含中子,故氢气中含有的中子数为0,故B错误;
C、甲烷为10电子分子,故0.5mol甲烷中含5NA个电子,故C正确;
D、醋酸为弱电解质,不能完全电离,故溶液中的离子个数小于2NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
14.丙烯可看作是乙烯分子中的一个氢原子被-CH3取代的产物,由乙烯推测丙烯的结构或性质,下列说法正确的是( )
①丙烯分子中3个碳原子在同一条直线上
②分子中所有原子都在同一平面上
③与HCl加成只生成一种产物
④丙烯可以使酸性高锰酸钾溶液褪色
⑤不溶于水,可溶于苯中
⑥能使溴的四氯化碳溶液褪色.
①丙烯分子中3个碳原子在同一条直线上
②分子中所有原子都在同一平面上
③与HCl加成只生成一种产物
④丙烯可以使酸性高锰酸钾溶液褪色
⑤不溶于水,可溶于苯中
⑥能使溴的四氯化碳溶液褪色.
| A. | ③④⑤ | B. | ①②⑤ | C. | ④⑤⑥ | D. | ②⑤⑥ |
12.某有机物的结构简式为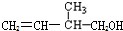 ,下列关于该有机物的叙述不正确的是( )
,下列关于该有机物的叙述不正确的是( )
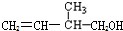 ,下列关于该有机物的叙述不正确的是( )
,下列关于该有机物的叙述不正确的是( )| A. | 能与金属钠发生反应并放出氢气 | |
| B. | 此有机物中有三种官能团:碳碳双键、羟基、甲基 | |
| C. | 能在催化剂作用下与H2发生加成反应 | |
| D. | 在浓H2SO4催化下能与乙酸发生酯化反应 |
19.有aXn-和bYm+两种单原子离子,它们的电子层结构相同,下列关系式或化学式不正确是( )
| A. | a+n=b-m | B. | X的氢化物化学式为HnX或XHn | ||
| C. | a<b | D. | Y的氧化物化学式为YOm |
9.下列说法正确的是( )
| A. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 | |
| B. | 工艺师利用盐酸刻蚀石英制作艺术品 | |
| C. | 二氧化硅可用于制备光导纤维 | |
| D. | 化学家采用玛瑙研砵磨擦固体反应物进行无溶剂合成,玛瑙的主要成分是硅酸盐 |
16.工业上一般在恒容密闭容器中采用下列反应合成甲醇:
CO(g)+2H2(g)?CH3OH(g)△H
(1)判断反应达到平衡状态的依据是(填字母序号,下同)CD.
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(2)如表所列数据是反应在不同温度下的化学平衡常数(K).
①由表中数据判断△H<(填“>”、“=”或“<”)0;
②某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为80%,此时的温度为250℃.
(3)要提高CO的转化率,可以采取的措施是DF.
A.升温 B.加入催化剂
C.增加CO的浓度 D.加入H2加压
E.加入惰性气体加压 F.分离出甲醇
(4)300℃时,在一定的压强下,5mol CO与足量的H2在催化剂的作用下恰好完全反应变化的热量为454kJ.在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
下列说法正确的是D.
A.2c1>c3 B.a+b<90.8
C.2p2<p3 D.α1+α3<1.
CO(g)+2H2(g)?CH3OH(g)△H
(1)判断反应达到平衡状态的依据是(填字母序号,下同)CD.
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(2)如表所列数据是反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为80%,此时的温度为250℃.
(3)要提高CO的转化率,可以采取的措施是DF.
A.升温 B.加入催化剂
C.增加CO的浓度 D.加入H2加压
E.加入惰性气体加压 F.分离出甲醇
(4)300℃时,在一定的压强下,5mol CO与足量的H2在催化剂的作用下恰好完全反应变化的热量为454kJ.在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1mol CO、2mol H2 | 1mo l CH3OH | 2mol CH3OH | |
| 平衡时数据 | CH3OH的 浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | a kJ | b kJ | c kJ | |
| 体系压强(Pa) | p1 | p2 | p3 | |
| 反应物转化率 | α1 | α2 | α3 | |
A.2c1>c3 B.a+b<90.8
C.2p2<p3 D.α1+α3<1.
13.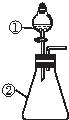 用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
 用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )| 选項 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 氢氧化钠稀溶液 | 硫酸铝铵溶液 | 立即产生白色沉淀 |
| B | 氢氧化钠浓溶液 | 用砂纸打磨过的镁条 | 立即产生大量无色气体 |
| C | 浓硫酸 | 铜粉 | 立即产生刺激性气味气体 |
| D | 盐酸 | 较浓的硝酸亚铁溶液 | 无明显现象 |
| A. | A | B. | B | C. | C | D. | D |
14.已知阿伏加德罗常数的值为NA,则下列说法正确的是( )
| A. | 1 mol/L CuCl2溶液中含有的Cl-的个数为2NA | |
| B. | 16 g甲烷中含有的共用电子对数为NA | |
| C. | 常温常压,46 gNO2与N2O4的混合气体中含有的原子数为3NA | |
| D. | 4.6 g Na与适量氧气完全反应生成Na2O、Na2O2的混合物中含有的阴离子数大于0.1NA |