题目内容
在常温下,氯化银的Ksp为1.8×10-10,溴化银的Ksp为5.0×10-13,请回答下列问题:
(1)在常温下的氯化银固体和氯化银共存的饱和溶液里,氯化银的物质的量浓度是(假设溶液的密度为1g?mL-1) .
(2)若常温下的氯化银固体和氯化银饱和溶液里液体的体积是1L,向其中加入39.1mg溴化钠并进行搅拌、静置(假设溶液的体积不变),试通过计算说明氯化银沉淀能否转化为溴化银沉淀.
(1)在常温下的氯化银固体和氯化银共存的饱和溶液里,氯化银的物质的量浓度是(假设溶液的密度为1g?mL-1)
(2)若常温下的氯化银固体和氯化银饱和溶液里液体的体积是1L,向其中加入39.1mg溴化钠并进行搅拌、静置(假设溶液的体积不变),试通过计算说明氯化银沉淀能否转化为溴化银沉淀.
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:(1)依据氯化银溶液中存在的沉淀溶解平衡结合氯化银的溶度积常数解答;
(2)依据氯化银、溴化银的溶度积常数可知溴化银溶解度小于氯化银,依据溴化银溶度积常数结合溶度积规则判断.
(2)依据氯化银、溴化银的溶度积常数可知溴化银溶解度小于氯化银,依据溴化银溶度积常数结合溶度积规则判断.
解答:
解:(1)氯化银溶液中存在溶解平衡:AgCl(s)?Ag+(aq)+Cl-(aq),
设银离子浓度为x,则:
AgCl(s)?Ag+(aq)+Cl-(aq)
x x
KSP=[Ag+][Cl-]=1.8×10-10(mol/L)2
x2=1.8×10-10(mol/L)2
解得x=1.3×10-5mol/L
所以c(AgCl)=c(Ag+)=c(Cl-)=1.3×10-5mol/L,
故答案为:1.3×10-5mol/L;
(2)39.1mg溴化银的物质的量为0.0391g÷103g/mol=3.8×10-4mol,所以c(Br-)=3.8×10-4mol/L,
氯化银饱和溶液中C(AgCl)=C(Ag+)=C(Cl-)=1.3×10-5mol/L;
加入溴化钠时,Qc(AgBr)=C(Ag+)C(Br-)=1.3×10-5mol/L×3.8×10-4mol/L=4.9×10-9(mol/L)2,大于5.0×10-13,QC>Ksp,依据溶度积规则可知:氯化银可以转化为溴化银沉淀;
答:氯化银沉淀能否转化为溴化银沉淀.
设银离子浓度为x,则:
AgCl(s)?Ag+(aq)+Cl-(aq)
x x
KSP=[Ag+][Cl-]=1.8×10-10(mol/L)2
x2=1.8×10-10(mol/L)2
解得x=1.3×10-5mol/L
所以c(AgCl)=c(Ag+)=c(Cl-)=1.3×10-5mol/L,
故答案为:1.3×10-5mol/L;
(2)39.1mg溴化银的物质的量为0.0391g÷103g/mol=3.8×10-4mol,所以c(Br-)=3.8×10-4mol/L,
氯化银饱和溶液中C(AgCl)=C(Ag+)=C(Cl-)=1.3×10-5mol/L;
加入溴化钠时,Qc(AgBr)=C(Ag+)C(Br-)=1.3×10-5mol/L×3.8×10-4mol/L=4.9×10-9(mol/L)2,大于5.0×10-13,QC>Ksp,依据溶度积规则可知:氯化银可以转化为溴化银沉淀;
答:氯化银沉淀能否转化为溴化银沉淀.
点评:本题考查了难溶电解质沉淀溶解平衡,为高考热门考点,明确溶度积常数的意义及溶度积规则是解题关键,题目难度较大.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
将固体NH4I置于密闭容器中,在某温度下发生反应:NH4I(固)?NH3(气)+HI(气); 2HI(气)?H2(气)+I2(气).当反应达到平衡时,c(H2)=0.5mol?L-1,c (HI)=4mol?L-1,则氨气的浓度为( )
| A、3.5 mol?L-1 |
| B、4 mol?L-1 |
| C、4.5 mol?L-1 |
| D、5 mol?L-1 |
下列关于药物的使用说法正确的是( )
| A、虽然药物能治病,但大部分药物有毒副作用 |
| B、使用青霉素时,直接静脉注射可以不用进行皮肤敏感试验 |
| C、长期大量使用阿司匹林可预防疾病,没有副作用 |
| D、麻黄碱有镇静催眠的效果 |

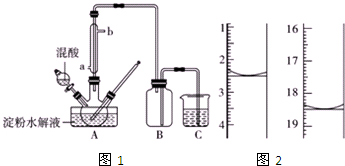 淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图1所示(加热,搅拌和仪器固定装置均已略去)
淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图1所示(加热,搅拌和仪器固定装置均已略去)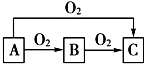 ABC是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物略去),回答下列问题:
ABC是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物略去),回答下列问题: