题目内容
在反应3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O中,当有1mol铜被氧化时,被还原的硝酸为( )
| A、8mol | ||
B、
| ||
| C、2mol | ||
D、
|
考点:氧化还原反应
专题:氧化还原反应专题
分析:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O中,3molCu被氧化,还原的硝酸为2mol,以此计算.
解答:
解:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O中,生成Cu(NO3)2体现酸的酸性,由电子守恒及原子守恒可知,3molCu被氧化,还原的硝酸为2mol,
则有1mol铜被氧化时,被还原的硝酸为
mol,
故选D.
则有1mol铜被氧化时,被还原的硝酸为
| 2 |
| 3 |
故选D.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,注意酸性、氧化剂的判断的方法,侧重分析能力、计算能力的考查,题目难度不大.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
在下列化合物中,既能在熔化状态,又能在溶液状态导电的物质是( )
| A、NaCl |
| B、冰醋酸 |
| C、CH3CH2OH |
| D、H2SO4 |
地壳中含量最多的元素是( )
| A、铝 | B、铁 | C、氧 | D、硅 |
下列分离或除杂方法不正确的是( )
| A、用分液法分离水和酒精 |
| B、用蒸馏法分离苯和溴苯 |
| C、用结晶法除去硝酸钾中的氯化钠杂质 |
| D、用饱和NaHCO3溶液除去CO2中混有的少量HCl气体 |
 某有机物A的结构简式如图所示,某同学对其可能具有的化学性质进行了如下预测
某有机物A的结构简式如图所示,某同学对其可能具有的化学性质进行了如下预测①可以使酸性高锰酸钾溶液褪色
②可以和NaOH溶液反应
③在一定条件下可以和乙酸发生反应
④在一定条件下可以发生消去反应
⑤在一定条件下可以和新制Cu(OH)2反应
⑥遇FeCl3溶液可以发生显色反应.其中正确的是( )
| A、①②③⑥ | B、①②③⑤ |
| C、①②③④ | D、①②④⑤ |
已知1g氢气在氧气中完全燃烧生成气态水,放出热量120.9kJ,则( )
| A、反应的热化学方程式:2H2(g)+O2(g)=2H2O(g)△H=+483.6 kJ?mol-1 |
| B、氢气的燃烧热为241.8 kJ?mol-1 |
| C、1 mol H2O(l)的能量大于1 mol H2O(g)的能量 |
| D、2 mol H2和1 mol O2的能量总和大于2 mol H2O(g)的能量 |
下列说法正确的为( )
| A、含有共价键的化合物称为共价化合物 |
| B、共价化合物里只存在共价键 |
| C、离子化合物里只存在离子键 |
| D、离子化合物只含有离子键的化合物 |
下列碱金属(IA族中的金属)性质的递变规律,随着核电荷数的递增,下列叙述错误的是( )
| A、单质的熔沸点依次升高 |
| B、原子半径依次增大 |
| C、单质的还原性依次增强 |
| D、氧化物对应的水化物碱性依次增强 |
结构为 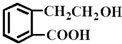 的有机物可以通过不同的反应得到下列四种物质:
的有机物可以通过不同的反应得到下列四种物质:
①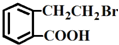 ②
②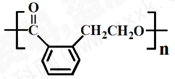 ③
③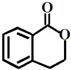 ④
④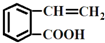
生成这四种有机物的反应类型依次为( )
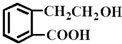 的有机物可以通过不同的反应得到下列四种物质:
的有机物可以通过不同的反应得到下列四种物质:①
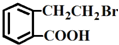 ②
② ③
③ ④
④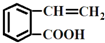
生成这四种有机物的反应类型依次为( )
| A、酯化、取代、缩聚、取代 |
| B、取代、取代、加聚、消去 |
| C、取代、缩聚、酯化、消去 |
| D、取代、加成、酯化、消去 |