��Ŀ����
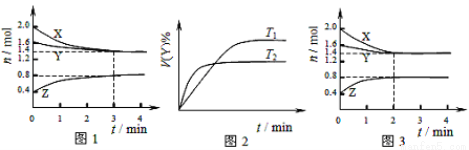
T ��ʱ��2L�ݻ�������ܱ�������ʹX(g)��Y(g)������Ӧ����Z(g)����Ӧ������X��Y��Z ��Ũ�ȱ仯��ͼ1��ʾ�������������������䣬�¶ȷֱ�ΪT1��T2ʱ��Y������ٷֺ�����ʱ��Ĺ�ϵ��ͼ2��ʾ�������н��۴�����ǣ� ��
A�������з����ķ�Ӧ�ɱ�ʾΪ��3X(g)+Y(g)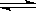 2Z(g)
2Z(g)
B��ͼ1 ��Ӧ����ǰ3min�ڣ���X��ʾ�ķ�Ӧ����v(X)��0.1mol/(L��min)
C�����ı䷴Ӧ������ʹ��Ӧ������ͼ3��ʾ����ı��������ʹ�ô���
D�����������������䣬�����¶ȣ���ѧƽ�����淴Ӧ�����ƶ�
D
��������
���������A. ����ͼ1��֪����ͬ��ʱ����X��С0.6��Y����0.2��Z����0.4�����ո������ʵ�Ũ�ȶ����ٷ����仯�����Ը÷�Ӧ�ǿ��淴Ӧ�������з����ķ�Ӧ�ɱ�ʾΪ��3X(g)+Y(g) 
 2Z(g)����ȷ��B��ͼ1 ��Ӧ����ǰ3min�ڣ���X��ʾ�ķ�Ӧ����v(X)��(0.6mol��2L)��3min=0.1mol/(L��min)����ȷ��C.���ڸı䷴Ӧ������Ӧ���ʼӿ죬�����˴ﵽƽ������Ҫ��ʱ�䣬�������ʵ�ƽ�⺬�����䣬��ı��������ʹ�ô�������ȷ��D������ͼ2��֪���¶�ΪT2ʱ���ȴﵽ�жϣ������������¶ȣ���ѧ��Ӧ���ʼӿ죬����T2>T1�����������¶Ⱥ�Y��ƽ�⺬�����ͣ�˵�������¶ȣ�ƽ��������Ӧ�����ƶ�������ƽ���ƶ�ԭ���������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ�������ӦΪ���ȷ�Ӧ������
2Z(g)����ȷ��B��ͼ1 ��Ӧ����ǰ3min�ڣ���X��ʾ�ķ�Ӧ����v(X)��(0.6mol��2L)��3min=0.1mol/(L��min)����ȷ��C.���ڸı䷴Ӧ������Ӧ���ʼӿ죬�����˴ﵽƽ������Ҫ��ʱ�䣬�������ʵ�ƽ�⺬�����䣬��ı��������ʹ�ô�������ȷ��D������ͼ2��֪���¶�ΪT2ʱ���ȴﵽ�жϣ������������¶ȣ���ѧ��Ӧ���ʼӿ죬����T2>T1�����������¶Ⱥ�Y��ƽ�⺬�����ͣ�˵�������¶ȣ�ƽ��������Ӧ�����ƶ�������ƽ���ƶ�ԭ���������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ�������ӦΪ���ȷ�Ӧ������
���㣺���黯ѧ����ʽ��ȷ�����¶ȡ������Ի�ѧƽ���ƶ���Ӱ���֪ʶ��

��10�֣�ijʵ��С����0��50 mol��L-1NaOH��Һ��0��50 mol��L-1������Һ�����к��ȵIJⶨ��
������0��50 mol��L-1NaOH��Һ
��1����ʵ���д�ԼҪʹ��470 mL NaOH��Һ,������Ҫ����NaOH���� g��
��2����ͼ��ѡ�����NaOH��������Ҫ��������(����ĸ): ��
���� | ������ƽ | С�ձ� | ����ǯ | ������ | ҩ�� | ��Ͳ |
���� |
|
|
|
|
|
|
��� | a | b | c | d | e | f |
�ⶨ�к��ȣ���1��ʵ�����ϱ����ձ�(��С�����ձ�)����ĭ���ϡ���ĭ���ϰ塢��ͷ�ιܡ���Ͳ�����ᡢNaOH��Һ,��ȱ�ٵ�ʵ�鲣����Ʒ�� ��
��2��ȡ50 mL NaOH��Һ��30 mL������Һ����ʵ��,ʵ���������±���������д�±��еĿհ�:
ʵ�� ���� | ��ʼ�¶�t1/�� | ��ֹ�¶� t2/�� | �¶Ȳ�ƽ��ֵ (t2-t1)/�� | ||
H2SO4 | NaOH | ƽ��ֵ | |||
1 | 26��2 | 26��0 | 26��1 | 30��1 |
|
2 | 27��0 | 27��4 | 27��2 | 33��3 | |
3 | 25��9 | 25��9 | 25��9 | 29��8 | |
4 | 26��4 | 26��2 | 26��3 | 30��4 | |
�ڽ�����Ϊ0��50 mol��L-1NaOH��Һ��0��50 mol/L������Һ���ܶȶ���1 g/cm3,�кͺ�������Һ�ı�����c=��4��18��J/(g����)�����к��Ȧ�H= (ȡС�����һλ)��
������ʵ����ֵ�����57��3 kJ��mol-1��ƫ��,����ƫ���ԭ�������(����ĸ) ��
A��ʵ��װ�ñ��¡�����Ч���� B����ȡNaOH��Һ�����ʱ���Ӷ���
C���ֶ�ΰ�NaOH��Һ����ʢ�������С�ձ���
D�����¶ȼƲⶨNaOH��Һ��ʼ�¶Ⱥ�ֱ�ӲⶨH2SO4��Һ���¶�



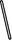


 B����̼��������Ӧ����
B����̼��������Ӧ����
 Fe(s)��CO2(g) ��H��0����֪��1 100 ��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K=0.263��
Fe(s)��CO2(g) ��H��0����֪��1 100 ��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K=0.263�� CH3OH(g)+H2O(g) ��H=��49.0KJ/mol���������Ϊ1L���ܱ������г���1mol CO2��3molH2����Ӧ�����в��CO2��CH3OH��g����Ũ����ʱ��ı仯��ͼ��ʾ��
CH3OH(g)+H2O(g) ��H=��49.0KJ/mol���������Ϊ1L���ܱ������г���1mol CO2��3molH2����Ӧ�����в��CO2��CH3OH��g����Ũ����ʱ��ı仯��ͼ��ʾ��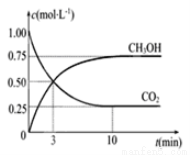
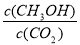 �������-------������ţ�
�������-------������ţ� NH3 (g)+H2O(g)+CO2(g)����H=+185.57 kJ��mol-1���Է�����,ԭ������ϵ���Է�������Ҷ����ӵķ���ת�������
NH3 (g)+H2O(g)+CO2(g)����H=+185.57 kJ��mol-1���Է�����,ԭ������ϵ���Է�������Ҷ����ӵķ���ת�������