题目内容
将氢氧化钡溶液滴入含1mol/L的KAl(SO4)2的明矾溶液中,当生成的沉淀的物质的量最多时,铝元素的主要存在形式为( )
| A、Al3+和Al(OH)3 |
| B、Al(OH)3 |
| C、AlO2- |
| D、AlO2-和Al(OH)3 |
考点:镁、铝的重要化合物
专题:元素及其化合物
分析:将氢氧化钡溶液滴入含1mol/L的KAl(SO4)2的明矾溶液中,随着氢氧化钡溶液的加入,铝离子和氢氧根离子先生成氢氧化铝沉淀,当铝离子和氢氧根离子恰好完全反应时,氢氧化铝的量最大,继续加入氢氧化钡溶液时,氢氧化铝和氢氧根离子反应生成偏铝酸根离子,氢氧化铝沉淀逐渐减少,可见明矾溶液中Al3+恰好沉淀完全时,生成沉淀的总的物质的量最大.
解答:
解:假设明矾溶液的体积为1L,则该明矾溶液中含有的离子:2molSO42-、1molAl3+和1molK+,向其中加入氢氧化钡溶液,先发生反应:2Al3++2SO42-+3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓,当铝离子和氢氧根离子恰好完全反应时,氢氧化铝的量最大,继续加入氢氧化钡溶液时,氢氧化铝和氢氧根离子反应生成偏铝酸根离子,氢氧化铝沉淀逐渐减少,发生反应:2Al(OH)3+Ba2++2OH-═2AlO2-+BaSO4↓+4H2O;可见明矾溶液中Al3+恰好沉淀完全时,生成沉淀的总的物质的量最大;故当生成的沉淀的物质的量最多时,铝元素的主要存在形式为:Al(OH)3,
故选B.
故选B.
点评:本题考查溶液中离子的共存,注意判比较Al3+和OH-恰好沉淀和SO42-全部转化成BaSO4沉淀时沉淀的量,题目难度中等.

练习册系列答案
相关题目
下列各组物质互为同系物的是( )
| A、苯和乙炔 |
| B、甲苯和二甲苯 |
| C、硝基苯和三硝基甲苯 |
| D、乙烯和丁二烯 |
13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构下面叙述正确的是( )
| A、13C与15N有相同的中子数 |
| B、13C与C60互为同位素 |
| C、15N与14N是N元素的两种同位素 |
| D、15N的核外电子数与中子数相同 |
某无色溶液中含有大量KOH,Na2CO3,Na2SO4,为验证其中阴离子,若限定只能使用试管和胶头滴管且只准取一次待测液,则加入试剂顺序正确的是( )
| A、BaCl2溶液,盐酸,酚酞 |
| B、BaCl2溶液,酚酞,盐酸 |
| C、酚酞,BaCl2溶液,盐酸 |
| D、酚酞,盐酸,BaCl2溶液 |
下列说法不正确的是( )
①用水鉴别苯、乙醇、溴苯;
②用饱和NaCl溶液除去溴苯中杂质Br2
③用酸性高锰酸钾鉴别乙酸、己烯和乙醇;
④用点燃的方法鉴别甲烷、乙烯
⑤用溴水可鉴别苯、己烯、乙醇、四氯化碳四种液体.
①用水鉴别苯、乙醇、溴苯;
②用饱和NaCl溶液除去溴苯中杂质Br2
③用酸性高锰酸钾鉴别乙酸、己烯和乙醇;
④用点燃的方法鉴别甲烷、乙烯
⑤用溴水可鉴别苯、己烯、乙醇、四氯化碳四种液体.
| A、①②⑤ | B、②③ |
| C、②③⑤ | D、①④⑤ |
25℃0.12mol?L-1的NaOH溶液和0.10mol?L-1盐酸等体积混合后,溶液的pH为( )(假设混合后溶液体积可以直接相加)
| A、pH=2 | B、pH=10 |
| C、pH=12 | D、pH=13 |
关于如图化学反应中的热效应,下列说法不正确的是( )


| A、图Ⅰ表示:反应物的总能量高于生成物的总能量,则反应放热,△H<0 |
| B、图Ⅱ表示:反应物的总能量低于生成物的总能量,则反应吸热,△H>0 |
| C、H2与O2化合生成液态水的能量变化过程可用图Ⅰ来表现 |
| D、符合图Ⅱ所示能量变化的化学反应,必须要加热才能发生 |
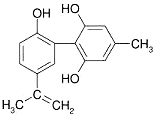 “人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如下图所示,有关该物质的说法正确的是( )
“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如下图所示,有关该物质的说法正确的是( )| A、该分子中的碳原子均为不饱和碳原子 |
| B、滴入酸性KMnO4溶液,观察紫色褪去,能证明结构中存在碳碳双键 |
| C、1mol该物质分别与浓溴水和H2反应,最多消耗Br2和H2的物质的量分别为4mol、7mol |
| D、遇FeCl3溶液呈紫色,因为该物质与苯酚属于同系物 |
 A、B、C、D、E是中学常见的单质,X是化合物.A、B均为常见的金属,且在地壳中的含量分别为金属元素的前两位;常温下C是气态非金属单质,可以燃烧;D是空气主要成份之一,可与C发生重要工业反应生成X;E是固体非金属单质,在氧气中燃烧时有明亮的蓝紫色火焰.根据上述物质的信息,回答下列有关问题:
A、B、C、D、E是中学常见的单质,X是化合物.A、B均为常见的金属,且在地壳中的含量分别为金属元素的前两位;常温下C是气态非金属单质,可以燃烧;D是空气主要成份之一,可与C发生重要工业反应生成X;E是固体非金属单质,在氧气中燃烧时有明亮的蓝紫色火焰.根据上述物质的信息,回答下列有关问题: