题目内容
下述实验能达到预期目的是( )
| 编号 | 实验内容 | 实验目的 |
| A | 将SO2通入酸性KMnO4溶液中 | 证明SO2具有漂白性 |
| B | Cl2能使湿润的红色布条褪色 | 证明Cl2具有漂白性 |
| C | 蓝矾固体放在浓硫酸中充分振荡,固体变为白色 | 证明浓硫酸具有吸水性 |
| D | 向某待测溶液中,加入BaCl2溶液,产生白色沉淀,然后再继续加入稀盐酸,沉淀不消失. | 证明待测溶液中含有SO42- |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价,物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题
分析:A.SO2通入酸性KMnO4溶液中,发生氧化还原反应;
B.Cl2能使湿润的红色布条褪色,是因氯气与水反应生成HClO;
C.蓝矾固体放在浓硫酸中充分振荡,浓硫酸具有吸水性,使晶体失去结晶水;
D.加入BaCl2溶液,产生白色沉淀,沉淀为硫酸钡或氯化银.
B.Cl2能使湿润的红色布条褪色,是因氯气与水反应生成HClO;
C.蓝矾固体放在浓硫酸中充分振荡,浓硫酸具有吸水性,使晶体失去结晶水;
D.加入BaCl2溶液,产生白色沉淀,沉淀为硫酸钡或氯化银.
解答:
解:A.SO2通入酸性KMnO4溶液中,发生氧化还原反应使高锰酸钾溶液褪色,S元素的化合价升高,体现二氧化硫的还原性,与漂白性无关,故A错误;
B.Cl2能使湿润的红色布条褪色,是因氯气与水反应生成HClO,HClO具有漂白性,而干燥的氯气不具有漂白性,故B错误;
C.蓝矾固体放在浓硫酸中充分振荡,浓硫酸具有吸水性,使晶体失去结晶水,则观察到蓝色变色白色,故C正确;
D.加入BaCl2溶液,产生白色沉淀,沉淀为硫酸钡或氯化银,再继续加入稀盐酸,沉淀不消失,原溶液中可能含银离子或硫酸根离子,但二者不能同时存在,故D错误;
故选C.
B.Cl2能使湿润的红色布条褪色,是因氯气与水反应生成HClO,HClO具有漂白性,而干燥的氯气不具有漂白性,故B错误;
C.蓝矾固体放在浓硫酸中充分振荡,浓硫酸具有吸水性,使晶体失去结晶水,则观察到蓝色变色白色,故C正确;
D.加入BaCl2溶液,产生白色沉淀,沉淀为硫酸钡或氯化银,再继续加入稀盐酸,沉淀不消失,原溶液中可能含银离子或硫酸根离子,但二者不能同时存在,故D错误;
故选C.
点评:本题考查化学实验方案的评价,为高频考点,涉及氧化还原反应、漂白性、浓硫酸的性质及离子检验等,把握物质的性质及化学反应原理为解答的关键,注意实验方案的评价性、操作性分析,选项C为易错点,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
25℃时,将1mol NH4NO3溶于水,向该溶液滴加b L氨水后溶液呈中性,据此判断下列说法中不正确的是(NH3?H2O的电离平衡常数取Kb=2×10-5mol?L-1)( )
| A、滴加氨水的过程中,水的电离平衡将正向移动 |
| B、滴加b L氨水后的溶液中,n(NH4+)=200 n(NH3?H2O)=1mol |
| C、所滴加氨水的浓度为0.005/b mol?L-1 |
| D、滴加b L氨水后的溶液中各离子浓度大小是:c(NH4+)=c(NO3-)>c(H+)=c(OH-) |
在醋酸的电离过程中,加入水会使下列比值增大的是( )
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
一定温度下,向容积固定不变的容器中充入a mol NO2,发生如下反应:2NO2(g)?N2O4(g),达到平衡后,再向该容器中充入amol NO2,达到平衡后与原来平衡比较正确的是( )
| A、NO2的转化率提高 |
| B、颜色变浅 |
| C、压强为原来的两倍 |
| D、平均相对分子质量减小 |
将20g铁粉放入一定量稀HNO3中,充分反应后放出气体2.24L(标准状况),剩余铁粉质量是( )
| A、14.4g | B、11.6g |
| C、8.8g | D、3.2g |
含有0.20mol Na2CO3的溶液120mL和200mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是( )
| A、1.5mol/L |
| B、2.0mol/L |
| C、0.18mol/L |
| D、0.24mol/L |
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在第三周期的元素中原子半径最大,元素D的合金是日常生活中常用的金属材料且元素D有两性.下列说法正确的是( )
| A、元素B、E组成的化合物BE4常温下呈气态 |
| B、一定条件下,元素C、D的最高价氧化物对应的水化物之间不能发生反应 |
| C、C、D、E的半径:C>D>E |
| D、化合物AE与CE是同类化合物 |
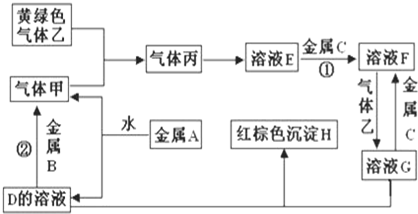
 观察图,回答问题.
观察图,回答问题.