题目内容
17.汽车尾气中的氮氧化物对大气造成污染,NO是其组成之一.已知N和O的核电荷数分别是7和8,则2个NO分子共含有的电子个数为( )| A. | 11 | B. | 15 | C. | 22 | D. | 30 |
分析 根据原子中核内质子数=核外电子数以及分子中电子数等于各原子中的电子数之和.
解答 解:N和O的核电荷数分别是7和8,N和O的核外电子数分别是7和8,则2个NO分子共含有的电子个数为2×(7+8)=30,
故选D.
点评 本题主要考查了分子中电子数等于各原子中的电子数之和,题目难度较小,注意把握原子中质子数与原子序数、电子数的关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列反应的离子方程式正确的是( )
| A. | Cu与FeCl3溶液反应:3Cu+2Fe3+═2Fe+3Cu2+ | |
| B. | 铁与稀H2SO4反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | Na与水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| D. | 向AlCl3溶液中滴入过量NaOH溶液:Al3++3OH-═Al(OH)3↓ |
6.在标准状况下将11.2L乙烯和乙炔的混合气体通入足量溴水中充分反应,测得有128g溴参加了反应,则乙烯和乙炔的物质的量之比为( )
| A. | 2:3 | B. | 1:2 | C. | 3:4 | D. | 4:5 |
7.化合物A、B是中学常见的物质,其阴、阳离子只能从表中选择:
(1)若A、B的水溶液均为无色,且A的水溶液呈强酸性,B的水溶液呈强碱性.混合后产生不溶于稀盐酸的白色沉淀及能使湿润的红色石蕊试纸变蓝色的气体.
①B的化学式为Ba(OH)2.
②A、B溶液混合加热反应的离子方程式H++SO42-+NH4++Ba2++2OH-$\frac{\underline{\;\;△\;\;}}{\;}$BaSO4↓+NH3↑+2H2O.
(2)若A的水溶液呈浅绿色,B的水溶液无色且其焰色反应为黄色.向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合亦无明显变化.则
①A的化学式为FeI2.
②经分析上述过程中溶液变黄的原因可能有两种(用离子方程式表示)
Ⅰ8H++2NO3-+6I-=2NO↑+3I2+4H2O;Ⅱ8H++2NO3-+6I-=2NO↑+3I2+4H2O和4H++NO3-+3Fe2+=NO↑+3Fe3++2H2O.
③请用一简易方法证明上述溶液变黄的原因取少量变黄溶液于试管中,滴加几滴KSCN溶液,若变红则Ⅱ合理(其他合理亦可).
| 阳离子 | K+、Na+、Fe2+、Ba2+、NH4+、Ca2+ |
| 阴离子 | OH-、NO3-、I-、HCO3-、AlO2-、HSO4- |
①B的化学式为Ba(OH)2.
②A、B溶液混合加热反应的离子方程式H++SO42-+NH4++Ba2++2OH-$\frac{\underline{\;\;△\;\;}}{\;}$BaSO4↓+NH3↑+2H2O.
(2)若A的水溶液呈浅绿色,B的水溶液无色且其焰色反应为黄色.向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合亦无明显变化.则
①A的化学式为FeI2.
②经分析上述过程中溶液变黄的原因可能有两种(用离子方程式表示)
Ⅰ8H++2NO3-+6I-=2NO↑+3I2+4H2O;Ⅱ8H++2NO3-+6I-=2NO↑+3I2+4H2O和4H++NO3-+3Fe2+=NO↑+3Fe3++2H2O.
③请用一简易方法证明上述溶液变黄的原因取少量变黄溶液于试管中,滴加几滴KSCN溶液,若变红则Ⅱ合理(其他合理亦可).
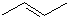 某有机物X的键线式为
某有机物X的键线式为 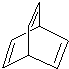
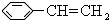 ,该芳香烃Z在一定条件下可发生聚合反应,写出其反应的化学方程
,该芳香烃Z在一定条件下可发生聚合反应,写出其反应的化学方程 .
.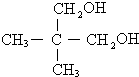 .
.
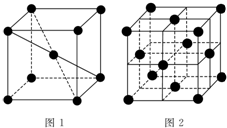 1 183K以下纯铁晶体的基本结构单元如图1所示,1 183K以上转变为图2所示结构的基本结构单元,在1中铁原子的配位数为8;其中为密堆积的是2(填“1”或“2”);1中的空间利用率为68%.
1 183K以下纯铁晶体的基本结构单元如图1所示,1 183K以上转变为图2所示结构的基本结构单元,在1中铁原子的配位数为8;其中为密堆积的是2(填“1”或“2”);1中的空间利用率为68%.