题目内容
7.NA为阿伏伽德罗常数,下列说法正确的是( )| A. | 标准状况下,11.2L的CH2Cl2所含的分子数为0.5NA | |
| B. | 28g乙烯所含共用电子对数目为4NA | |
| C. | 常温常压下,16gO2和O3的混合气体含有的氧原子数为NA | |
| D. | 1molCaC2所含阴离子数为2NA |
分析 A.标准状况下二氯甲烷的状态不是气体;
B.乙烯分子中含有6对共用电子对,28g乙烯的物质的量为1mol,含有6mol共用电子对;
C.氧气和臭氧分子中都只含有氧元素,根据n=$\frac{m}{M}$计算出混合物中含有氧原子的物质的量即可;
D.1mol碳化钙中只含有1mol阴离子.
解答 解:A.标况下CH2Cl2不是气体,不能使用标准状况下的气体摩尔体积计算,故A错误;
B.28g乙烯的物质的量为:$\frac{28g}{28g/mol}$=1mol,1mol乙烯分子中含有6mol共用电子对,所含共用电子对数目为6NA,故B错误;
C.16gO2和O3的混合气体中含有16g氧原子,含有的氧原子的物质的量为:$\frac{16g}{16g/mol}$=1mol,含有的氧原子数的为NA,故C正确;
D.1molCaC2含有1mol阴离子C22-,所含阴离子数为NA,故D错误;
故选C.
点评 本题考查阿伏加德罗常数的综合应用,题目难度中等,注意明确标准状况下气体摩尔体积的使用条件,熟练掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
17.某反应过程能量变化如图所示,下列说法正确的是( )


| A. | 改变催化剂,可改变该反应的活化能 | |
| B. | 该反应为放热反应,热效应等于E 1-E 2 | |
| C. | 反应过程 a 有催化剂参与 | |
| D. | 有催化剂条件下,反应的活化能等于 E 1+E 2 |
18.下列关于电解质的说法正确的是( )
| A. | 铜能导电但属于非电解质 | |
| B. | 氯化氢气体不能导电,所以氯化氢是非电解质 | |
| C. | 电解质不一定能导电 | |
| D. | SO2溶于水形成的溶液能导电,所以SO2是电解质 |
15.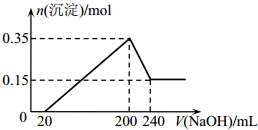 将一定质量的镁和铝混合物投入200mL硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示.则下列说法不正确的是( )
将一定质量的镁和铝混合物投入200mL硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示.则下列说法不正确的是( )
 将一定质量的镁和铝混合物投入200mL硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示.则下列说法不正确的是( )
将一定质量的镁和铝混合物投入200mL硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示.则下列说法不正确的是( )| A. | 生成的氢气在标准状况下的体积为11.2L | |
| B. | 最初20mLNaOH溶液用于中和过量的硫酸 | |
| C. | 硫酸的物质的量浓度为2.5mol/L | |
| D. | 镁和铝的总质量为9g |
2.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1.7g羟基(-OH)中含有的电子数为NA | |
| B. | 6.4g由S2、S4、S8组成的混 合物含硫原子数为0.2NA | |
| C. | 标准状况下2.24L己烷分子中含有1.9NA对共用电子 | |
| D. | 标准状况下,2.24LCl2通入足量H2O或NaOH溶液中转移的电子数均为0.1NA |
12.关于反应CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2的说法不正确的是( )
| A. | 该反应是氧化还原反应 | B. | Cu是氧化剂 | ||
| C. | CO是还原剂 | D. | 该反应中有电子转移 |
19.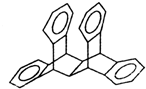 科罗拉多大学的克利斯托(S.Cristol)等人合成了一种有机分子,这种分子让他想起罗马的两面神Janus--罗马的守门神,克利斯托的同事迈金泰(Macintyre)就建议将该分子叫做Janusene.该有机物的结构简式如图所示,下列说法正确的是
科罗拉多大学的克利斯托(S.Cristol)等人合成了一种有机分子,这种分子让他想起罗马的两面神Janus--罗马的守门神,克利斯托的同事迈金泰(Macintyre)就建议将该分子叫做Janusene.该有机物的结构简式如图所示,下列说法正确的是
( )
 科罗拉多大学的克利斯托(S.Cristol)等人合成了一种有机分子,这种分子让他想起罗马的两面神Janus--罗马的守门神,克利斯托的同事迈金泰(Macintyre)就建议将该分子叫做Janusene.该有机物的结构简式如图所示,下列说法正确的是
科罗拉多大学的克利斯托(S.Cristol)等人合成了一种有机分子,这种分子让他想起罗马的两面神Janus--罗马的守门神,克利斯托的同事迈金泰(Macintyre)就建议将该分子叫做Janusene.该有机物的结构简式如图所示,下列说法正确的是( )
| A. | 该有机物的一氯代物只有4种(不包括立体异构) | |
| B. | 该有机物完全燃烧生成CO2和H2O的物质的量之比为15:11 | |
| C. | 该有机物属于苯的同系物 | |
| D. | 该有机物只能发生取代反应而不能发生加成反应 |
16.氨基钠和氢化钠与水反应的化学方程式如下:①NaNH2+H2O═NaOH+NH3↑②NaH+H2O═NaOH+H2↑,下列叙述正确的是( )
| A. | 氨基钠和氢化钠与盐酸反应都只生成一种盐 | |
| B. | 方程式②中,每生成1mol H2转移1 mol电子 | |
| C. | 熔融氢化钠不导电 | |
| D. | 方程式①中,氨基钠是还原剂 |
