题目内容
在溶液中能大量共存的一组离子或分子是( )
| A、NH4+、H+、NO3-、HCO3- |
| B、K+、Al(OH)4-、SO42-、NH3?H2O |
| C、Na+、K+、SO32-、ClO- |
| D、Na+、CH3COO-、SO42-、H+ |
考点:离子共存问题
专题:
分析:A.氢离子与碳酸氢根离子反应生成二氧化碳气体;
B.四种离子之间不发生反应,在溶液中能够大量共存;
C.次氯酸根离子在溶液中能够氧化亚硫酸根离子;
D.氢离子与次氯酸根离子结合生成弱电解质醋酸.
B.四种离子之间不发生反应,在溶液中能够大量共存;
C.次氯酸根离子在溶液中能够氧化亚硫酸根离子;
D.氢离子与次氯酸根离子结合生成弱电解质醋酸.
解答:
解:A.H+、HCO3-之间发生反应生成二氧化碳气体和水,在溶液中不能大量共存,故A错误;
B.K+、Al(OH)4-、SO42-、NH3?H2O之间不反应,在溶液中可以大量共存,故B正确;
C.SO32-、ClO-之间发生氧化还原反应,在溶液中不能大量共存,故C错误;
D.CH3COO-、H+之间反应生成醋酸,在溶液中不能大量共存,故D错误;
故选B.
B.K+、Al(OH)4-、SO42-、NH3?H2O之间不反应,在溶液中可以大量共存,故B正确;
C.SO32-、ClO-之间发生氧化还原反应,在溶液中不能大量共存,故C错误;
D.CH3COO-、H+之间反应生成醋酸,在溶液中不能大量共存,故D错误;
故选B.
点评:本题考查离子共存的正误判断,为中等难度的试题,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间,能发生络合反应的离子之间(如 Fe3+和 SCN-)等.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
 向500mL某碳酸钠溶液中逐滴加入1mol/L的盐酸,测得溶液中溶液中Cl─、HCO3─的物质的量随加入盐酸体积的关系如图所示,则下列说法中正确的是 ( )
向500mL某碳酸钠溶液中逐滴加入1mol/L的盐酸,测得溶液中溶液中Cl─、HCO3─的物质的量随加入盐酸体积的关系如图所示,则下列说法中正确的是 ( )| A、Oa段与ab段反应的离子方程式均为:CO32-+H+=HCO3- |
| B、该碳酸钠溶液的物质的量浓度为0.5mol/L |
| C、b点时,滴加盐酸的体积为600mL |
| D、b点时生成CO2的物质的量为0.3 mol |
根据原子结构及元素周期律的知识,下列叙述正确的是( )
| A、由于相对分子质量:HCl>HF,故沸点:HCl>HF |
| B、硅处于金属与非金属的过渡位置,硅可用作半导体材料 |
| C、由于氮元素的最低化合价只有-3价,故NH5这种物质不可能存在 |
| D、Cl-、S2-、Ca2+、K+半径逐渐减小 |
下列离子方程式正确的是( )
| A、向次氯酸钙溶液通入少量CO2:2ClO-+H2O+CO2=CO32-+2HClO |
| B、向明矾溶液中加入足量Ba(OH)2溶液:Al3++2SO42-+4OH-+2Ba2+=2BaSO4↓+[Al(OH)4]- |
| C、向FeCl3溶液中加入足量单质锌:Zn+2Fe3+=Zn2++2Fe2+ |
| D、向NaHSO4中滴加Ba(OH)2溶液至中性:H++SO42-+OH-+Ba2+=BaSO4↓+H2O |
某课外实验小组设计的下列实验不合理的是( )
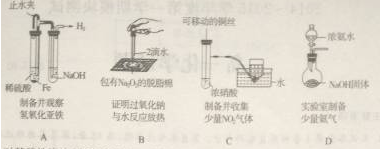

| A、A | B、B | C、C | D、D |
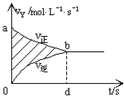 在容积固定的1L密闭容器里,进行可逆反应:X(g)+Y(g)?2Z(g),并达到平衡,在此过程中,以Y的浓度改变表示的反应速率v(正)、v(逆)与时间t的关系如图,结合题设条件,图中阴影部分面积不能表示( )
在容积固定的1L密闭容器里,进行可逆反应:X(g)+Y(g)?2Z(g),并达到平衡,在此过程中,以Y的浓度改变表示的反应速率v(正)、v(逆)与时间t的关系如图,结合题设条件,图中阴影部分面积不能表示( )| A、Z的浓度增加 |
| B、Y的物质的量减少 |
| C、X的浓度减少 |
| D、Y的浓度减少 |

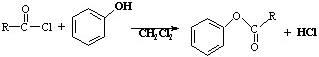 .
.