题目内容
5.下列表达式正确的是( )| A. | S2+的电子式为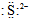 | B. | 碳原子的电子式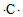 | ||
| C. | 氯原子的结构示意图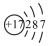 | D. | F-的结构示意图为 |
分析 A.阴离子应用中括号括起来,并标注所带电荷数;
B.碳原子最外层4个电子;
C.氯原子核内17个质子,核外3个电子层,从内到外依次容纳2,8,7个电子;
D.氟离子最外层8个电子.
解答 解:A.S2-的核外有18个电子,最外层有8个电子,其电子式为 ,故A错误;
,故A错误;
B.碳原子的电子式为: ,故B错误;
,故B错误;
C.氯原子核内17个质子,核外3个电子层,从内到外依次容纳2,8,7个电子,离子方程式: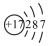 ,故C正确;
,故C正确;
D.氟离子核内有9个质子,核外有10个电子,氟离子的结构示意图为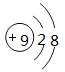 ,故D错误;
,故D错误;
故选:C.
点评 本题考查常见化学用语的使用,侧重考查学生对原子的结构示意图、电子式等知识的理解与掌握,并能在解题中灵活应用,有利于培养学生正确使用化学用语的习惯.

练习册系列答案
相关题目
2.如图所示,下列实验操作方法正确的是( )
| A. |  检测容量瓶是否漏水的方法 | B. |  给溶液加热 | ||
| C. |  放回滴瓶 | D. | 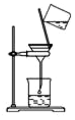 过滤 |
13.下列叙述正确的是( )
| A. | 物质的量浓度为0.5 mol/L的MgCl2溶液,含有Cl- 个数为NA | |
| B. | V mL硫酸铁溶液中含有mg SO42-,则Fe3+的物质的量浓度为6.94m/V mol•L-1 | |
| C. | 将58.5 g NaCl溶解于1 L水中配成溶液,所得溶液的物质的量浓度为1 mol•L-1 | |
| D. | 用36.5%的浓盐酸(密度为1.25g•cm-3)配制成浓度为0.1mol•L-1的稀盐酸240mL,所需浓盐酸的体积为1.9mL |
17.设 NA为阿伏加德罗常数值,下列有关叙述正确的是( )
| A. | 将 78gNa2O2 与过量 CO2反应转移的电子数为 2NA | |
| B. | 1mol N2与 4mol H2反应生成的 NH3 分子数为 2NA | |
| C. | 标准状况下,2.24L SO3 中所含原子数为 0.4 NA | |
| D. | 标准状况下,18g D2O 中所含电子数为 9 NA |
14.“瓦斯”爆炸会严重威胁煤矿安全,下列说法正确的是( )
| A. | “瓦斯”的主要成分为一氧化碳 | B. | 爆炸过程放出大量热量 | ||
| C. | 爆炸过程有氧气参与反应 | D. | 爆炸过程吸收大量热量 |
15.用固体样品配制一定物质的量浓度的溶液,下列图示对应的有关操作规范的是( )
| A. | 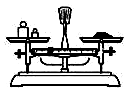 称量 称量 | B. | 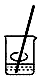 溶解 | C. | 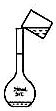 转移 | D. | 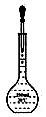 定容 |