题目内容
下列实验的现象与对应结论均正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
| B | 常温下将Al片放入浓硝酸中 | 无明显现象 | Al与浓硝酸不反应 |
| C | 将一小块Na放入无水乙醇中 | 产生气泡 | Na能置换出醇中的氢 |
| D | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:
分析:A.水蒸气通过灼热的铁粉,生成四氧化三铁和氢气;
B.常温下浓硫酸、浓硝酸遇到铝、铁发生钝化现象,生成一薄层致密的氧化物薄膜阻止反应进行;
C.钠和乙醇反应置换羟基中的氢原子;
D.浓硫酸具有脱水性使蔗糖脱水生成碳变黑,碳和浓硫酸反应生成二氧化碳和二氧化硫气体.
B.常温下浓硫酸、浓硝酸遇到铝、铁发生钝化现象,生成一薄层致密的氧化物薄膜阻止反应进行;
C.钠和乙醇反应置换羟基中的氢原子;
D.浓硫酸具有脱水性使蔗糖脱水生成碳变黑,碳和浓硫酸反应生成二氧化碳和二氧化硫气体.
解答:
解:A.水蒸气通过灼热的铁粉,生成四氧化三铁和氢气,铁粉变为黑色,故A错误;
B.常温下将Al片放入浓硝酸中,无明显变化,铝和浓硝酸发生钝化现象,发生反应生成一薄层致密的氧化物薄膜阻止反应进行,表现了强氧化性,故B错误;
C.将一小块Na放入无水乙醇中,产生气泡,Na能置换出醇羟基中的氢,故C正确;
D.将浓硫酸滴到蔗糖表面,固体变黑膨胀,浓硫酸具有脱水性使蔗糖脱水生成碳变黑,碳和浓硫酸反应生成二氧化碳和二氧化硫气体表现浓硫酸的氧化性,故D正确.
故选CD.
B.常温下将Al片放入浓硝酸中,无明显变化,铝和浓硝酸发生钝化现象,发生反应生成一薄层致密的氧化物薄膜阻止反应进行,表现了强氧化性,故B错误;
C.将一小块Na放入无水乙醇中,产生气泡,Na能置换出醇羟基中的氢,故C正确;
D.将浓硫酸滴到蔗糖表面,固体变黑膨胀,浓硫酸具有脱水性使蔗糖脱水生成碳变黑,碳和浓硫酸反应生成二氧化碳和二氧化硫气体表现浓硫酸的氧化性,故D正确.
故选CD.
点评:本题考查化学实验方案的评价,明确常见物质的性质及发生的反应为解答的关键,注意发生的氧化还原反应及因果关系的判断,题目难度不大.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
下列说法不正确的是( )
A、 的分子式为C17H24O3 的分子式为C17H24O3 |
| B、水溶液中氨基酸在等电点时的溶解度最小.不同的氨基酸达到等电点的pH不同,故可以通过调节溶液pH分离某些氨基酸 |
C、有机硅聚醚( )可由单体 )可由单体  和 和 缩聚而成 缩聚而成 |
| D、等质量的甲醇、甲醛、甲醚完全燃烧时的耗氧量依次递增 |
某无色溶液中,常温下由水电离出的c(H+)=1×10-14 mol/L,则该溶液中一定能大量共存的离子是( )
| A、Al3+、Na+、MnO4-、SO42- |
| B、Na+、Ag+、Cl-、NO3-、 |
| C、Na+、K+、Cl-、NO3- |
| D、K+、Ba2+、Cl-、HCO3- |
下列所描述的现象与氧化还原反应有关的是( )
| A、银白色的钠放置于空气中变暗 |
| B、白色的CuSO4粉末遇水变蓝 |
| C、Na2CO3溶液中加入CaCl2溶液产生白色沉淀 |
| D、活性炭使红墨水褪色 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、在常温常压下,2.8 gN2和CO的混合气体所含电子数为1.4NA | ||
| B、标准状况下,22.4 LCCl4含有的分子数目为NA | ||
C、1 L O.1 mol?L-1NaHCO3溶液中含有0.1NA个HCO
| ||
| D、在电解精炼粗铜的过程中,当转移电子数为 NA时,阳极溶解32 g |
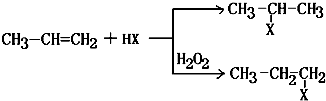 (X)为卤素原子
(X)为卤素原子 的物质,该物质是一种香料.
的物质,该物质是一种香料.
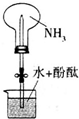 化学是一门以实验为基础的科学.
化学是一门以实验为基础的科学.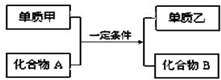 置换反应的通式可表示为如图:单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:
置换反应的通式可表示为如图:单质甲、乙和化合物A、B为中学常见物质,请回答下列问题: