题目内容
17.已知有如下反应:①2BrO3-+Cl2═Br2+2ClO3-,
②ClO3-+5Cl-+6H+═3Cl2↑+3H2O,
③3Cl2+I2+6H2O=2HIO3+10HCl.
下列各微粒氧化能力由强到弱的顺序正确的是( )
| A. | Cl2>BrO3->ClO3->HIO3 | B. | ClO3->BrO3->HIO3>Cl2 | ||
| C. | BrO3->Cl2>ClO3->HIO3 | D. | BrO3->ClO3->Cl2>HIO3 |
分析 在自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性.
解答 解:①中BrO3-是氧化剂,ClO3-是氧化产物,所以氧化性BrO3->ClO3-,
②中ClO3-是氧化剂,是Cl2氧化产物,所以氧化性ClO3->Cl2,
③中Cl2是氧化剂,HIO3是氧化产物,所以氧化性Cl2>IO3-,综上得氧化性顺序为BrO3->ClO3->Cl2>HIO3-.
故选D.
点评 本题考查了根据方程式来比较氧化性和还原性.解题的关键是根据化合价找出氧化剂、还原剂、氧化产物和还原产物.

练习册系列答案
相关题目
7.下列有关说法正确的是( )
| A. | 反应2CO(g)=2C(s)+O2(g)△H>0可以自发进行 | |
| B. | 放热反应在常温条件下一定很容易进行 | |
| C. | 平衡常数发生变化,化学平衡一定发生移动 | |
| D. | 化学平衡发生移动,平衡常数一定发生改变 |
8.下列叙述正确的是( )
| A. | 某醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b | |
| B. | 在滴有酚酞溶液的氨水中,加入NH4Cl至溶液恰好无色,则此时溶液pH<7 | |
| C. | 若1mL pH=1的盐酸与100mL NaOH溶液混合后,溶液的pH=7,则NaOH溶液的pH=11 | |
| D. | 1.0×10-3mol•L-1盐酸的pH=3.0;1.0×10-8mol•L-1盐酸的pH=8.0 |
12.某学生配制一定物质的量浓度的氢氧化钠溶液后,经测定发现溶液浓度偏高.该学生找出以下原因,其中会使溶液浓度偏高的是( )
| A. | 没有用蒸馏水洗烧杯2-3次,并将洗液移入容量瓶中 | |
| B. | 容量瓶刚用蒸馏水洗净,没有烘干 | |
| C. | 定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切 | |
| D. | 定容时俯视刻度线 |
9.通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一.对下列实验事实的解释正确的是( )
| 操作、现象 | 解释 | |
| A | 把生铁放置于潮湿的空气中,铁表面有一层红棕色的斑点 | 铁在潮湿的空气中易生成Fe(OH)3 |
| B | 向KI淀粉溶液中加入FeCl3溶液,溶液变蓝 | Fe3+能与淀粉发生显色反应 |
| C | 新制Fe(OH)2露置于空气中一段时间,白色物质变成了红褐色 | 说明Fe(OH)2易被O2氧化成Fe(OH)3 |
| D | 向稀硝酸中加入少量铁粉,有气泡产生 | 说明Fe置换出硝酸中的氢,生成了氢气 |
| A. | A | B. | B | C. | C | D. | D |
6.下列有关于乙醇的说法正确的是( )
| A. | 医用酒精的浓度通常为95% | |
| B. | Y(C2H5OH),W(C2H5ONa)可通过消去反应由Y得到W | |
| C. | 实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法 | |
| D. | 向无水乙醇中加入浓H2SO4,加热至170℃,产生的气体通入酸性KMnO4溶液,紫红色褪去,使溶液褪色的气体只是乙烯 |
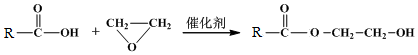
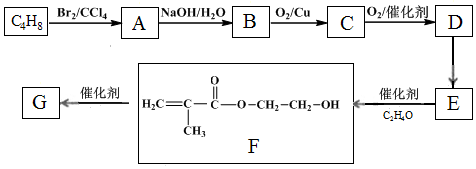
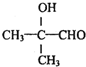 .
.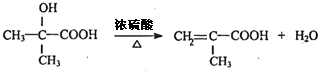 .
. .
.