题目内容
用18mol/L 浓硫酸配制250ml 3.0mol/L 稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③稀释④转移、洗涤⑤定容、摇匀
回答下列问题:
(1)配制时需选用的仪器主要有量筒、 、 、 、烧杯和试剂瓶.
(2)量取浓硫酸的体积是 mL,量取浓硫酸所用的量筒的规格是 .(从下列中选用 A.10mL B.25mL C.50mL D.100ml)
(3)简述第③步实验的操作
(4)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.所用的浓硫酸长时间放置在密封不好的容器中
B.所用过的烧杯、玻璃棒未洗涤
C.定容时俯视溶液的液凹面 .
①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③稀释④转移、洗涤⑤定容、摇匀
回答下列问题:
(1)配制时需选用的仪器主要有量筒、
(2)量取浓硫酸的体积是
(3)简述第③步实验的操作
(4)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.所用的浓硫酸长时间放置在密封不好的容器中
B.所用过的烧杯、玻璃棒未洗涤
C.定容时俯视溶液的液凹面
考点:溶液的配制
专题:实验题
分析:(1)根据配制250ml 3.0mol/L 稀硫酸的步骤选用仪器,然后判断还缺少的仪器;
(2)溶液稀释过程中溶质的物质的量不变,据此计算出需要浓硫酸的体积;根据计算结果判断量筒的规格;
(3)浓硫酸密度大于水、稀释过程中放热大量热,所以应该将浓硫酸缓缓加入水中,顺序不能颠倒;
(4)根据c=
可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量n和溶液的体积V引起的,误差分析时,关键要看配制过程中引起n和V怎样的变化:若n比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若n比理论值大,或V比理论值小时,都会使所配溶液浓度偏大.
(2)溶液稀释过程中溶质的物质的量不变,据此计算出需要浓硫酸的体积;根据计算结果判断量筒的规格;
(3)浓硫酸密度大于水、稀释过程中放热大量热,所以应该将浓硫酸缓缓加入水中,顺序不能颠倒;
(4)根据c=
| n |
| V |
解答:
解:(1)配制250ml 3.0mol/L 稀硫酸的步骤为:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,配制过程中选用的仪器有:量筒、烧杯、玻璃棒、胶头滴管、250mL容量瓶等,还缺少的仪器为:250mL容量瓶、胶头滴管、玻璃棒,
故答案为:250mL容量瓶;胶头滴管;玻璃棒;
(2)250ml 3.0mol/L稀硫酸,需要18mol/L的浓硫酸的体积为:
≈0.0417L=41.7mL,需要选用50mL的量筒,所以C正确,
故答案为:41.7;C;
(3)稀释浓硫酸的操作方法为:将浓硫酸沿烧杯内壁缓缓注入水中,并用玻璃棒不断搅拌,
故答案为:将浓硫酸沿烧杯内壁缓缓注入水中,并用玻璃棒不断搅拌;
(4)A.所用的浓硫酸长时间放置在密封不好的容器中,浓硫酸被稀释,浓度减小,则配制的硫酸中溶质的物质的量减小,配制的溶液浓度偏小,
故答案为:偏小;
B.所用过的烧杯、玻璃棒未洗涤,导致配制的溶液中溶质的物质的量偏小,配制的溶液浓度偏小,
故答案为:偏小;
C.定容时俯视溶液的液凹面,导致加入的蒸馏水体积偏小,配制的溶液体积偏小,溶液浓度偏大,
故答案为:偏大.
故答案为:250mL容量瓶;胶头滴管;玻璃棒;
(2)250ml 3.0mol/L稀硫酸,需要18mol/L的浓硫酸的体积为:
| 3.0mol/L×0.25L |
| 18mol/L |
故答案为:41.7;C;
(3)稀释浓硫酸的操作方法为:将浓硫酸沿烧杯内壁缓缓注入水中,并用玻璃棒不断搅拌,
故答案为:将浓硫酸沿烧杯内壁缓缓注入水中,并用玻璃棒不断搅拌;
(4)A.所用的浓硫酸长时间放置在密封不好的容器中,浓硫酸被稀释,浓度减小,则配制的硫酸中溶质的物质的量减小,配制的溶液浓度偏小,
故答案为:偏小;
B.所用过的烧杯、玻璃棒未洗涤,导致配制的溶液中溶质的物质的量偏小,配制的溶液浓度偏小,
故答案为:偏小;
C.定容时俯视溶液的液凹面,导致加入的蒸馏水体积偏小,配制的溶液体积偏小,溶液浓度偏大,
故答案为:偏大.
点评:本题考查了配制一定物质的量浓度的溶液的方法,题目难度中等,注意掌握配制一定物质的量浓度的溶液方法,试题侧重对学生能力的培养和解题方法的指导和训练,有利于培养学生的逻辑思维能力和严谨的规范实验操作能力;该题的难点在于误差分析,注意明确误差分析的方法与技巧.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
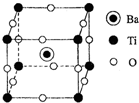 钛及其化合物被广泛应用于飞机、火箭、卫星、舰艇、医疗以及石油化工等邻域.下面是用金红石(主要成分为TiO2)制备金属钛和钛酸钡的流程.
钛及其化合物被广泛应用于飞机、火箭、卫星、舰艇、医疗以及石油化工等邻域.下面是用金红石(主要成分为TiO2)制备金属钛和钛酸钡的流程.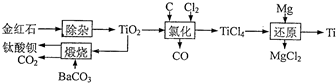
 在一密闭体系中发生下列反应A(g)+3B(g)?2C(g)△H<0,如图是某一时间段中反应速率与反应进程的曲线关系,完成下列问题:
在一密闭体系中发生下列反应A(g)+3B(g)?2C(g)△H<0,如图是某一时间段中反应速率与反应进程的曲线关系,完成下列问题:

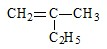
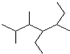 的名称
的名称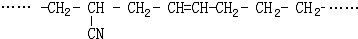 则合成它的单体是
则合成它的单体是