题目内容
11.一定条件下,体积为10L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g)?Z(g),经60s达到平衡,生成0.3molZ.下列说法正确的是( )| A. | 以X浓度变化表示的反应速率为0.0001mol/(L•s) | |
| B. | 将容器体积变为20L,Z的平衡浓度变为原来的$\frac{1}{2}$ | |
| C. | 若增大压强,则物质Y的转化率减小 | |
| D. | 若升高温度,X的体积分数增大,则该反应的△H<0 |
分析 经60s达到平衡,生成0.3molZ,则
2X(g)+Y(g)?Z(g),
开始 1 1 0
转化 0.6 0.3 0.3
平衡 0.4 0.7 0.3
A.结合v=$\frac{△c}{△t}$计算;
B.将容器体积变为20L,压强减小,平衡逆向移动;
C.增大压强,平衡正向移动;
D.若升高温度,X的体积分数增大,可知升高温度平衡逆向移动.
解答 解:经60s达到平衡,生成0.3molZ,则
2X(g)+Y(g)?Z(g),
开始 1 1 0
转化 0.6 0.3 0.3
平衡 0.4 0.7 0.3
A.X浓度变化表示的反应速率为$\frac{\frac{0.6mol}{10L}}{60s}$=0.001mol/(L•s),故A错误;
B.将容器体积变为20L,压强减小,平衡逆向移动,则Z的平衡浓度小于原来的$\frac{1}{2}$,故B错误;
C.增大压强,平衡正向移动,则物质Y的转化率增大,故C错误;
D.若升高温度,X的体积分数增大,可知升高温度平衡逆向移动,正反应为放热反应,则该反应的△H<0,故D正确;
故选D.
点评 本题考查化学平衡的计算,为高频考点,把握速率计算、化学平衡移动等为解答的关键,侧重分析与计算能力的考查,注意选项B为解答的易错点,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.某化学课外兴趣小组学生用如图1所示的装置探究苯和液溴的反应并制备溴苯,有关数据如表.
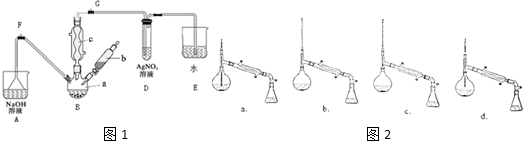
请分析后回答下列问题.
(1)打开G处止水夹,关闭F处止水夹,在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,向a中滴入几滴溴,有白色烟雾产生,继续滴加至液溴滴完,三颈烧瓶中发生反应的化学方程式为 .
.
(2)液溴滴完后,打开F处止水夹,关闭G处止水夹,一段时间后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的Fe;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤,再经过分液,(填实验操作名称)分离出的粗溴苯,再中加入少量的无水氯化钙,静置、过滤.
(3)经以上分离操作后,要把粗溴苯进一步提纯,进行的实验操作中,仪器选择及安装都正确的是如图2:b(填字母)锥形瓶中得到的主要物质是苯(填物质名称).
(4)D中试管内出现的现象是溶液中有淡黄色沉淀生成,某同学认为不能因此证明苯和液溴的反应是取代反应,若要证明,需改进的实验操作是在B、D间安装一个装有CCl4溶液的洗气瓶.
(5)本实验存在一个明显不足之处是制溴苯过程中装置D、E中的溶液容易倒吸入装置B,导致实验失败.
| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |

请分析后回答下列问题.
(1)打开G处止水夹,关闭F处止水夹,在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,向a中滴入几滴溴,有白色烟雾产生,继续滴加至液溴滴完,三颈烧瓶中发生反应的化学方程式为
 .
.(2)液溴滴完后,打开F处止水夹,关闭G处止水夹,一段时间后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的Fe;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤,再经过分液,(填实验操作名称)分离出的粗溴苯,再中加入少量的无水氯化钙,静置、过滤.
(3)经以上分离操作后,要把粗溴苯进一步提纯,进行的实验操作中,仪器选择及安装都正确的是如图2:b(填字母)锥形瓶中得到的主要物质是苯(填物质名称).
(4)D中试管内出现的现象是溶液中有淡黄色沉淀生成,某同学认为不能因此证明苯和液溴的反应是取代反应,若要证明,需改进的实验操作是在B、D间安装一个装有CCl4溶液的洗气瓶.
(5)本实验存在一个明显不足之处是制溴苯过程中装置D、E中的溶液容易倒吸入装置B,导致实验失败.
2.一定温度下,1mol X和n mol Y在体积为2L的密闭容器中发生如下反应:X(g)+Y(g)?2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z.下列说法正确的是( )
| A. | 用X表示此反应的反应速率是0.1amol•L-1•min-1 | |
| B. | 当混合气体的压强不再发生变化时,说明反应达到平衡状态 | |
| C. | 向平衡后的体系中加入1 mol M,平衡向逆反应方向移动 | |
| D. | 向上述平衡体系中再充入1 mol X,v正增大,v逆减小,平衡正向移动 |
19.表明金属甲的活动性比金属乙的活动性强的叙述正确的是( )
| A. | 在氧化还原反应中,甲比乙失电子多 | |
| B. | 同价态阳离子,甲比乙的氧化性强 | |
| C. | 甲能与冷水反应而乙不能 | |
| D. | 将甲、乙组成原电池时,乙为负极 |
16.将 4molA气体和 2molB气体在 2L 固定体积的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)?2C(g).若经2s后测得 C 的浓度为 0.6mol•L-1,现有下列几种说法,其中正确的是( )
| A. | 用物质 A 表示的反应的平均速率为 0.3 mol•L-1•s-1 | |
| B. | 用物质 B 表示的反应的平均速率为 0.6 mol•L-1•s-1 | |
| C. | 2 s 时物质 A 的转化率为70% | |
| D. | 2 s 时物质 B 的浓度为 0.7 mol•L-1 |
3.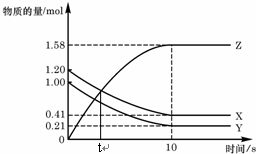 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图,下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图,下列描述正确的是( )
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图,下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图,下列描述正确的是( )| A. | t秒时该反应达到化学平衡状态 | |
| B. | 反应开始到10 s,X的物质的量浓度减少了0.79mol/L | |
| C. | 反应开始到10s时,Y的转化率为79.0% | |
| D. | 反应的化学方程式为:X(g)+Y(g)?2Z(g) |
20.x、y、z为三种气体,把a mol x和b mol y充入一密闭容器中,发生反应,x+2y?2z达到平衡时,若它们的物质的量满足n(x)+n(y)=n(z),则y的转化率为( )
| A. | $\frac{a+b}{5×100%}$ | B. | $\frac{2(a+b)}{5b×100%}$ | C. | $\frac{200(a+b)}{5b}$% | D. | $\frac{(a+b)}{5a×100%}$ |