题目内容
下列关于SiO2晶体说法不正确的是( )
| A、60gSiO2中含Si-O键的个数为2NA |
| B、晶体中微粒堆积不服从紧密堆积原理的原因是共价键具有饱和性和方向性 |
| C、SiO2晶体的熔沸点较干冰高是由于晶体类型不同 |
| D、与硅原子最近的四个氧原子构成一个正四面体 |
考点:不同晶体的结构微粒及微粒间作用力的区别,硅和二氧化硅
专题:化学键与晶体结构,碳族元素
分析:A、1molSiO2晶体存在4molSi-O键;
B、共价键具有饱和性和方向性导致了原子晶体中原子的堆积不属于密堆积;
C、原子晶体的熔沸点高于分子晶体的熔沸点;
D、晶体中一个硅原子和最近的四个氧原子形成四面体结构,四个氧原子处于同一四面体的四个顶点.
B、共价键具有饱和性和方向性导致了原子晶体中原子的堆积不属于密堆积;
C、原子晶体的熔沸点高于分子晶体的熔沸点;
D、晶体中一个硅原子和最近的四个氧原子形成四面体结构,四个氧原子处于同一四面体的四个顶点.
解答:
解:A、1molSiO2晶体存在4molSi-O键,所以60gSiO2晶体即1mol含有4molSi-O键,即为4NA个,故A错误;
B、共价键具有饱和性和方向性导致了原子晶体中原子的堆积不属于密堆积,故B正确;
C、二氧化硅属于原子晶体,干冰属于分子晶体,原子晶体的熔沸点高于分子晶体的熔沸点,故C正确;
D、晶体中一个硅原子和最近的四个氧原子形成四面体结构,四个氧原子处于同一四面体的四个顶点,故D正确;
故选A.
B、共价键具有饱和性和方向性导致了原子晶体中原子的堆积不属于密堆积,故B正确;
C、二氧化硅属于原子晶体,干冰属于分子晶体,原子晶体的熔沸点高于分子晶体的熔沸点,故C正确;
D、晶体中一个硅原子和最近的四个氧原子形成四面体结构,四个氧原子处于同一四面体的四个顶点,故D正确;
故选A.
点评:本题主要考查了二氧化硅晶体结构,二氧化硅晶属于原子晶体,难度不大,掌握原子晶体的结构是解题的关键.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
下列化合物,按其晶体的熔点由低到高排列正确的是( )
| A、SiO2 CsCl I2 Br2 |
| B、SiO2 CsCl Br2 I2 |
| C、CsCl SiO2 I2 Br2 |
| D、Br2 I2 CsCl SiO2 |
光照条件下,下列各组物质中几乎没有反应的是( )
| A、甲烷与溴蒸气 |
| B、甲烷和氧气 |
| C、氢气和氯气 |
| D、甲烷和氯气 |
下列物质分类正确的是( )
| A、苯和溴苯均为芳香烃 |
| B、酚醛树脂和聚乙烯均为体型高分子材料 |
| C、葡萄糖和麦芽糖均为还原性糖 |
| D、油脂和淀粉均为天然高分子化合物 |
下列实验装置或操作设计正确且能达到实验目的是.( )
A、 配制一定物质的量浓度的稀硫酸 |
B、 制取少量的Fe(OH)3胶体 |
C、 用H2SO4标准溶液滴定NaOH溶液 |
D、 称量NaOH固体 |
下列有关实验原理或操作的说法正确的是( )
| A、为得到较大的晶体颗粒,结晶时通常采用浓度较低,溶剂蒸发速度较慢或溶液冷却较慢的条件 |
| B、纸层析中,滤纸作为固定相,展开剂作为流动相 |
| C、过滤、结晶、灼烧、萃取、分液和蒸馏等都是常用的分离有机混合物的方法 |
| D、用硝酸银溶液可以鉴别NaCl溶液和NaNO2溶液 |





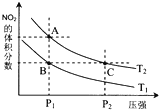 氮可形成多种氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是
氮可形成多种氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是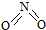 和
和 .实验测得N-N键键能为167kJ?mol-1,NO2中氮氧键的平均键能为466kJ?mol-1,N2O4中氮氧键的平均键能为438.5kJ?mol-1.
.实验测得N-N键键能为167kJ?mol-1,NO2中氮氧键的平均键能为466kJ?mol-1,N2O4中氮氧键的平均键能为438.5kJ?mol-1.