题目内容
常温下,在10mL 0.2mol/L某一元强酸HA的溶液中逐滴加入a mL 0.1mol/L的氨水,下列有关说法中正确的是( )
| A、当c(NH4+)=c(A-)时,a一定等于20 |
| B、当c(NH4+)>c(A-)时,a一定大于20 |
| C、当c(H+)=c(OH-)时,a一定小于20 |
| D、当pH=7时,c(NH4+)=c(A-)=c(H+)=c(OH-) |
考点:酸碱混合时的定性判断及有关ph的计算,弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:A.如果c(NH4+)=c(A-)时,根据电荷守恒得c(H+)=c(OH-),要使混合溶液呈中性,则氨水的物质的量稍微大些;
B.如果c(NH4+)>c(A-)时,则c(H+)<c(OH-),溶液中的溶质为一水合氨和NH4A;
C.当c(H+)=c(OH-)时,溶液呈中性,要使溶液呈中性,氨水的物质的量稍微大于HA;
D.常温下,当pH=7时,溶液呈中性则c(H+)=c(OH-),溶液中溶质为一水合氨和NH4A,水的电离程度很小.
B.如果c(NH4+)>c(A-)时,则c(H+)<c(OH-),溶液中的溶质为一水合氨和NH4A;
C.当c(H+)=c(OH-)时,溶液呈中性,要使溶液呈中性,氨水的物质的量稍微大于HA;
D.常温下,当pH=7时,溶液呈中性则c(H+)=c(OH-),溶液中溶质为一水合氨和NH4A,水的电离程度很小.
解答:
解:A.如果c(NH4+)=c(A-)时,根据电荷守恒得c(H+)=c(OH-),要使混合溶液呈中性,则氨水的物质的量稍微大些,所以a一定大于20,故A错误;
B.如果c(NH4+)>c(A-)时,则c(H+)<c(OH-),溶液中的溶质为一水合氨和NH4A,则氨水物质的量大于HA,所以a一定大于20,故B正确;
C.当c(H+)=c(OH-)时,溶液呈中性,根据A选项知,a一定大于20,故C错误;
D.常温下,当pH=7时,溶液呈中性则c(H+)=c(OH-),根据电荷守恒得c(NH4+)=c(A-),溶液中溶质为一水合氨和NH4A,水的电离程度离子浓度大小顺序是c(NH4+)=c(A-)>c(H+)=c(OH-),故D错误;
故选B.
B.如果c(NH4+)>c(A-)时,则c(H+)<c(OH-),溶液中的溶质为一水合氨和NH4A,则氨水物质的量大于HA,所以a一定大于20,故B正确;
C.当c(H+)=c(OH-)时,溶液呈中性,根据A选项知,a一定大于20,故C错误;
D.常温下,当pH=7时,溶液呈中性则c(H+)=c(OH-),根据电荷守恒得c(NH4+)=c(A-),溶液中溶质为一水合氨和NH4A,水的电离程度离子浓度大小顺序是c(NH4+)=c(A-)>c(H+)=c(OH-),故D错误;
故选B.
点评:本题考查了离子浓度大小比较,明确溶质的性质再结合溶液酸碱性、电荷守恒分析解答,根据离子浓度确定溶液中溶质为易错点.

练习册系列答案
相关题目
下列粒子中,与H3O+所含质子数、电子数相等,且化学键类型相同的粒子是( )
| A、Na+ |
| B、NH4+ |
| C、Ne |
| D、NH3 |
下面是有关弱酸的电离平衡常数.
结合数据,分析下列有关说法,其中错误的是( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A、1 mol?L-1的溶液中,pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) |
| B、升高温度时,HCN溶液中HCN的电离平衡正向移动,c(H+)增大,电离平衡常数增大 |
| C、向稀醋酸中加入相同浓度的HCN溶液,醋酸的电离平衡正向移动 |
| D、饱和H2CO3溶液中c(H+)与 c(CO32-)的比值大于2 |
Harbermann等设计出利用Desulfovibrio desulfurcan菌种生成的硫化物作为介体的微生物燃料电池,电池内部有质子(即H+)通过,该系统不经任何维护可连续运行5年.该电池的负极反应式为S2-+4H2O-8e-=SO42-+8H+.下列说法中正确的是( )
| A、若有1.12 L氧气参与反应,则有0.2 mol电子发生转移 |
| B、质子由正极移向负极 |
| C、该电池的总反应为S2-+2O2=SO42- |
| D、正极的电极反应式为2O2+8e-+4H2O=8OH- |
对于0.1mol/L的醋酸水溶液,下列说法中错误的是( )
| A、加入少量醋酸钠固体,则醋酸根离子浓度减少 |
| B、若加入少量冰醋酸,则氢离子浓度增大 |
| C、若加入少量的NaOH,则醋酸根离子浓度增大 |
| D、若加入少量的盐酸,则醋酸根离子浓度减少 |
下列说法正确的是( )
| A、1mol O的质量是32g/mol |
| B、H2O的摩尔质量是18g |
| C、1mol H2O的质量是18 g/mol |
| D、CO2的摩尔质量是44 g/mol |
下列表达不正确的是( )
| A、反应2NO2═O2+2NO;△H=+116.2kJ/mol 任何情况非自发 |
| B、Na2CO3溶液中:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) |
| C、表示碳燃烧热的热化学方程式为 C(s)+O2(g)=CO2(g);△H=-393.5kJ/mol |
| D、等物质的量的KHCO3和Ba(OH)2的溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O |
用下列实验装置完成对应的实验,能达到实验目的是( )
A、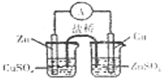 构成钢管原电池 |
B、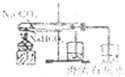 比较NaHCO3和Na2CO3的热稳定性 |
C、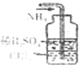 吸收多余的NH3 |
D、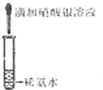 配制银氨溶液 |
常温下,柠檬水溶液的PH是3,其中的C(OH-)是( )
| A、0.1mol/L |
| B、1.0×10-3 mol/L |
| C、1.0×10-11mol/L |
| D、1.0×10-7mol/L |