题目内容
4.下列溶液一定显酸性的是( )| A. | 含H+的溶液 | B. | pH=6的溶液 | ||
| C. | c(OH-)<c(H+)的溶液 | D. | 能与Al(OH)3反应的溶液 |
分析 只要溶液中存在c(OH-)<c(H+),则该溶液一定呈酸性,要根据溶液中c(OH-)、c(H+)相对大小判断溶液酸碱性,不能根据溶液pH、与Al(OH)3是否反应来判断溶液酸碱性.
解答 解:A.任何电解质的水溶液中都含有H+,所以含H+的溶液不一定呈酸性,可能呈中性或碱性,故A错误;
B.100℃时纯水溶液pH=6,纯水溶液呈中性,所以温度未知时不能根据pH大小判断溶液酸碱性,故B错误;
C.只要溶液中存在c(OH-)<c(H+),则该溶液一定呈酸性,故C正确;
D.强酸、强碱溶液都能与Al(OH)3反应生成盐和水,所以能与Al(OH)3反应的溶液不一定呈酸性,故D错误;
故选C.
点评 本题考查溶液酸碱性判断,为高频考点,要根据溶液中c(OH-)、c(H+)相对大小判断溶液酸碱性,不能盲目的关键溶液pH判断溶液酸碱性,易错选项是B.

| A. | 量筒、酸式滴定管、水 | B. | 容量瓶、碱式滴定管、苯 | ||
| C. | 量筒、碱式滴定管、水 | D. | 容量瓶、酸式滴定管、四氯化碳 |
| A. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液变红 | |
| B. | Na2O与Na2O2组成元素相同、阴阳离子个数比相同,但跟水反应的产物不同 | |
| C. | 只存在共价键的物质一定是共价化台物、离子化合物中一定含有离子键 | |
| D. | 元素原子的最外层电子数越多,得电子能力越强,失电子能力越弱 |
| A. | 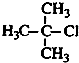 2-甲基-2-氯丙烷 | B. | 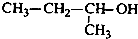 2-甲基-1-丙醇 | C. | 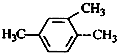 1,3,4-三甲苯 | D. | 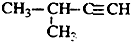 2-甲基-3-丁炔 |
| A. |  甘油 甘油 | B. | CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 | ||
| C. | 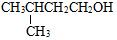 3-甲基-1-丁醇 3-甲基-1-丁醇 | D. | 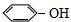 石碳酸 石碳酸 |
| A. | V(A)=0.15mol/(l•s) | B. | V(B)=0.6mol/(l•s) | C. | V(C)=0.45mol/(l•s) | D. | V(D)=4.0mol/(l•min) |
25℃时,有关物质的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | H2SO3 |
电离平衡常数K | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)电解质由强至弱顺序为_________________(用化学式表示,下同)。
(2)常温下,0.02 mol·L-1的CH3COOH溶液的电离度约为 ,体积为10mLpH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者 后者(填“>”、“<”或“=”)。
(3)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶 液
液 中结合H+的能力由大到小的顺序为_____________。
中结合H+的能力由大到小的顺序为_____________。
(4)NaHSO3溶液显酸性的原因___________________________(离子方程式配适当文字叙述),其溶液中离子浓度由大到小的关系是_______________.
