题目内容
按要求完成下列反应的方程式.
(1)写出漂白粉长期暴露在空气中变质所发生的两个化学反应方程式 , .
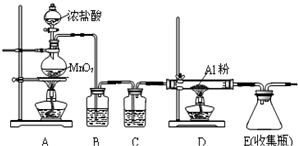
(2)写出工业上用氧化铝和二氧化锰两种物质制取金属锰的两个化学反应方程式 , .
(3)从海水中提取镁,其中一步是将氢氧化镁与盐酸反应,写出该反应的离子反应方程式 ;从铝土矿中提取铝,其中一步是在偏铝酸钠溶液中通入足量CO2反应,写出该反应的离子反应方程式 .
(1)写出漂白粉长期暴露在空气中变质所发生的两个化学反应方程式
(2)写出工业上用氧化铝和二氧化锰两种物质制取金属锰的两个化学反应方程式
(3)从海水中提取镁,其中一步是将氢氧化镁与盐酸反应,写出该反应的离子反应方程式
考点:氯、溴、碘及其化合物的综合应用,海水资源及其综合利用,铝的化学性质
专题:元素及其化合物
分析:(1)漂白粉置露在空气中会变质,发生漂白粉与二氧化碳、水的反应及次氯酸分解反应;
(2)可以用铝热反应来冶炼金属锰;
(3)氢氧化镁可以和盐酸之间反应产生氯化镁和水,偏铝酸钠溶液中通入足量CO2产物是氢氧化铝和碳酸氢钠.
(2)可以用铝热反应来冶炼金属锰;
(3)氢氧化镁可以和盐酸之间反应产生氯化镁和水,偏铝酸钠溶液中通入足量CO2产物是氢氧化铝和碳酸氢钠.
解答:
解:(1)漂白粉置露在空气中会变质,发生漂白粉与二氧化碳、水的反应及次氯酸分解反应,反应分别为①Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO、②2HClO
2HCl+O2↑,
故答案为:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;2HClO
2HCl+O2↑.
(2)高温下电解氧化铝的熔融物可以得到金属铝2Al2O3
2Al+3O2↑,利用铝热反应:金属铝和二氧化锰之间的反应来冶炼金属锰,即4Al+3MnO2
3Mn+2Al2O3,故答案为:2Al2O3
2Al+3O2↑;4Al+3MnO2
3Mn+2Al2O3;
(3)氢氧化镁可以和盐酸之间反应产生氯化镁和水,实质是:Mg(OH)2+2H+=Mg2++2H2O,偏铝酸钠溶液中通入足量CO2产物是氢氧化铝和碳酸氢钠,实质是:CO2+2H2O+AlO2-=Al(OH)3↓+HCO3-,故答案为:Mg(OH)2+2H+=Mg2++2H2O;CO2+2H2O+AlO2-=Al(OH)3↓+HCO3-.
| ||
故答案为:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;2HClO
| ||
(2)高温下电解氧化铝的熔融物可以得到金属铝2Al2O3
| ||
| ||
| ||
| ||
(3)氢氧化镁可以和盐酸之间反应产生氯化镁和水,实质是:Mg(OH)2+2H+=Mg2++2H2O,偏铝酸钠溶液中通入足量CO2产物是氢氧化铝和碳酸氢钠,实质是:CO2+2H2O+AlO2-=Al(OH)3↓+HCO3-,故答案为:Mg(OH)2+2H+=Mg2++2H2O;CO2+2H2O+AlO2-=Al(OH)3↓+HCO3-.
点评:本题涉及漂白粉、含铝化合物的性质等知识,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
除去NaHCO3溶液中的少量杂质Na2CO3,所用试剂或方法是( )
| A、加热 |
| B、Ca(OH)2溶液 |
| C、通入过量的CO2 |
| D、NaOH溶液 |
 氢气是一种新型的绿色能源,又是一种重要的化工原料.
氢气是一种新型的绿色能源,又是一种重要的化工原料.