题目内容
完成下列离子反应方程式
(1)将铁粉投入到CuSO4溶液中
(2将Al2O3溶于稀盐酸中
(3)将金属铝投入到NaOH溶液中
(4)将Ba(OH)2溶液与H2SO4溶液混合 .
(1)将铁粉投入到CuSO4溶液中
(2将Al2O3溶于稀盐酸中
(3)将金属铝投入到NaOH溶液中
(4)将Ba(OH)2溶液与H2SO4溶液混合
考点:离子方程式的书写
专题:
分析:(1)铁与铜离子发生置换反应生成亚铁离子和铜单质;
(2)氧化铝与盐酸反应生成氯化铝和水;
(3)铝与氢氧化钠溶液反应生成偏铝酸钠与氢气;
(4)氢氧化钡溶液与稀硫酸反应生成了硫酸钡沉淀和水.
(2)氧化铝与盐酸反应生成氯化铝和水;
(3)铝与氢氧化钠溶液反应生成偏铝酸钠与氢气;
(4)氢氧化钡溶液与稀硫酸反应生成了硫酸钡沉淀和水.
解答:
解:(1)铁粉和硫酸铜能发生置换反应生成铜,同时生成硫酸亚铁,反应的离子方程式为:Fe+Cu2+=Cu+Fe2+,
故答案为:Fe+Cu2+=Fe2++Cu;
(2)氧化铝能够与稀盐酸反应生成氯化铝和水,反应的离子方程式为:Al2O3+6H+=2Al3++3H2O,
故答案为:Al2O3+6H+=2Al3++3H2O;
(3)氢氧化钠溶液反应生成偏铝酸钠与氢气,反应离子方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
(4)氢氧化钡与硫酸都是可溶性的强电解质,溶液中电离出的钡离子与硫酸根离子生成硫酸钡沉淀,氢氧根离子与氢离子反应生成了弱电解质水,反应的离子方程式为:Ba2++SO42-+2H++2OH-═BaSO4↓+2H2O,
故答案为:Ba2++SO42-+2H++2OH-═BaSO4↓+2H2O.
故答案为:Fe+Cu2+=Fe2++Cu;
(2)氧化铝能够与稀盐酸反应生成氯化铝和水,反应的离子方程式为:Al2O3+6H+=2Al3++3H2O,
故答案为:Al2O3+6H+=2Al3++3H2O;
(3)氢氧化钠溶液反应生成偏铝酸钠与氢气,反应离子方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
(4)氢氧化钡与硫酸都是可溶性的强电解质,溶液中电离出的钡离子与硫酸根离子生成硫酸钡沉淀,氢氧根离子与氢离子反应生成了弱电解质水,反应的离子方程式为:Ba2++SO42-+2H++2OH-═BaSO4↓+2H2O,
故答案为:Ba2++SO42-+2H++2OH-═BaSO4↓+2H2O.
点评:本题考查了离子方程式的书写,题目难度中等,注意掌握离子方程式的书写方法,本题侧重对学生基础知识的训练和检验,有利于提高学生灵活运用基础知识能力.

练习册系列答案
相关题目
向FeI2溶液中滴加适量氯水,将反应后溶液分3份,甲试管中滴加淀粉溶液,乙试管滴加KSCN溶液,丙试管中滴加酸性高锰酸钾溶液,下列说法正确的是( )
| A、若甲试管溶液呈蓝色,则乙试管溶液一定呈血红色 |
| B、若甲试管溶液呈蓝色,则乙试管溶液可能无明显现象 |
| C、乙试管溶液呈血红色,则甲试管溶液不可能呈蓝色 |
| D、甲试管溶液呈蓝色,丙试管中紫红色褪去,说明滴加氯水后的溶液中一定存在Fe3+和Fe2+ |
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:2NH3(g)?N2(g)+3H2(g)△H=+92.4kJ/mol.实验测得起始、平衡时的有关数据如下表:下列叙述正确的是( )
| 容器编号 | 起始时各物质 物质的量/mol | 平衡时反应中的能量变化 | ||
| NH3 | N2 | H2 | ||
| ① | 2 | 0 | 0 | 吸收热量a kJ |
| ② | 0 | 1 | 3 | 放出热量b kJ |
| ③ | 4 | 0 | 0 | 吸收热量c kJ |
| A、热量关系:a=b |
| B、①②③反应的平衡常数:③>①>② |
| C、达平衡时H2的体积分数:①>③ |
| D、①中的密度不再改变时说明反应已达到平衡状态 |
下列各组离子能大量共存的是( )
| A、Ag+ NO3- Cl- H+ |
| B、Ba2+ SO42- NO3- Na+ |
| C、Ba2+ Mg2+ NO3- Cl- |
| D、CO32- H+ OH- Ca2+ |
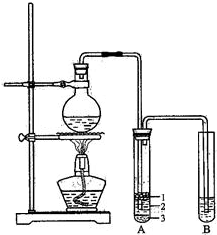 根据题意完成下列填空:有关数据列表如下:
根据题意完成下列填空:有关数据列表如下: