题目内容
用惰性电极电解一定质量的某浓度的KCl溶液,一段时间后停止电解.此时若加入73g10%的盐酸,所得溶液正好与原溶液完全相同,则电解过程中转移电子的物质的量约为( )
| A、0.2mol |
| B、1.7mol |
| C、7.5mol |
| D、7.7mol |
考点:电解原理
专题:电化学专题
分析:用惰性电极电解KCl溶液时,若加入73g10%的盐酸,所得溶液正好与原溶液完全相同,根据“析出什么加入什么”的原则知,知电解时阳极上有氢氧根离子和氯离子放电,阴极上氢离子放电,73g10%的盐酸中m(HCl)=73g×10%=7.3g,n(HCl)=
=0.2mol,m(H2O)=73g-7.3g=65.7g,n(H2O)=
3.65mol,根据氢原子守恒计算转移电子的物质的量.
| 7.3g |
| 36.5g/mol |
| 65.7g |
| 18g/mol |
3.65mol,根据氢原子守恒计算转移电子的物质的量.
解答:
解:用惰性电极电解KCl溶液时,若加入73g10%的盐酸,所得溶液正好与原溶液完全相同,根据“析出什么加入什么”的原则知,知电解时阳极上有氢氧根离子和氯离子放电,阴极上氢离子放电,73g10%的盐酸中m(HCl)=73g×10%=7.3g,n(HCl)=
=0.2mol,m(H2O)=73g-7.3g=65.7g,n(H2O)=
3.65mol,根据H原子守恒得n(H)=n(HCl)+2n(H2O)=0.2mol+(2×3.65)mol=7.5mol,每个H+得一个电子生成H原子,所以转移电子的物质的量为7.5mol,
故选C.
| 7.3g |
| 36.5g/mol |
| 65.7g |
| 18g/mol |
3.65mol,根据H原子守恒得n(H)=n(HCl)+2n(H2O)=0.2mol+(2×3.65)mol=7.5mol,每个H+得一个电子生成H原子,所以转移电子的物质的量为7.5mol,
故选C.
点评:本题以电解原理为载体考查了物质的量的有关计算,明确阳极上放电的离子是解本题关键,根据H原子和转移电子之间的关系式计算,注意守恒思想的运用,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在标准状况下,用铂电极电解CuSO4溶液,当阴极产生12.8g铜时,阳极放出的气体是( )
| A、1.12L H2 |
| B、1.12L O2 |
| C、2.24L H2 |
| D、2.24L O2 |
下列离子方程式正确的是( )
| A、氢氧化铁与盐酸反应:OH-+H+=H2O |
| B、金属钠和水反应:2Na+2H2O=2Na++2OH-+H2↑ |
| C、硫酸溶液中加入氢氧化钡溶液:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| D、向稀硫酸溶液中投入铁粉:2Fe+6H+=2Fe3++3H2↑ |
下列说法中,正确的是( )
| A、粗硅制备单晶硅不涉及氧化还原反应 |
| B、工艺师利用盐酸刻蚀石英制作艺术品 |
| C、水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
| D、硅是目前人类将太阳能转变为电能的重要材料 |
下列说法中,正确的是( )
| A、元素周期表中的第ⅠA族元素全部是碱金属元素 |
| B、元素周期表中的第ⅦA族元素全部是非金属元素 |
| C、元素周期表中的0族元素最外层电子数都是8个 |
| D、元素周期表划分为7个周期18个族 |
在反应 Cl2+KOH(浓)═KClO3+KCl+H2O (未配平)中,氧化剂与还原剂物质的量之比为( )
| A、1:5 | B、4:1 |
| C、5:1 | D、1:4 |
下列化学用语表达正确的是( )
| A、甲烷的标准燃烧热△H=-890.3 kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3 kJ?mol-1 |
B、丙烯的键线式: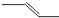 |
| C、一定条件下,某密闭容器中充入2mol SO2(g)和1molO2(g),达到平衡后,放出QkJ热量,则该条件下的热化学方程式为:2SO2(g)+O2(g)?2SO3(g )△H=-Q kJ?mol-1 |
| D、乙烯的结构简式:CH2CH2 |
某学生实验仪器的选择及数据记录,都合理的是( )
| A、酸碱中和滴定时,用10mL量筒量取10.00mL待测液 |
| B、用托盘天平称量25.20gNaCl固体 |
| C、常温条件下,用广泛pH试纸测得纯水的pH为7.0 |
| D、用500mL容量瓶配制480mL0.1000mol/LNaOH溶液 |
下列溶液中的氯离子的物质的量浓度与50mL 1mol?L-1的AlCl3溶液中氯离子物质的量浓度相等的是( )
| A、25mL 3 mol?L-1的KCl |
| B、75 mL 1.5 mol?L-1的CaCl2 |
| C、150 mL 1 mol?L-1的NaCl |
| D、100 mL 2 mol?L-1的FeCl3 |