题目内容
8.请选用合适的试剂及操作方法除去下列物质中的杂质,并将相应的序号填写到表格中.所加试剂有:①NaOH溶液 ②盐酸 ③过量铁粉 ④Ba(OH)2溶液
除杂的操作方法有:A.萃取 B.加热 C.过滤 D.重结晶 E.点燃.
| 编号 | 物质 | 杂质(少量) | 试 剂 | 除杂操作方法 |
| (1) | Na2CO3固体 | NaHCO3 | - | |
| (2) | Fe | Al | ||
| (3) | FeSO4 | CuSO4 | ||
| (4) | NaOH | Na2CO3 | ||
| (5) | KNO3 | NaCl | - |
分析 (1)Na2CO3固体较稳定,加热条件下不分解,NaHCO3不稳定受热易分解生成Na2CO3;
(2)Al易溶于NaOH溶液,但Fe不易溶于NaOH溶液;
(3)CuSO4能和Fe反应生成FeSO4;
(4)Na2CO3能和适量Ba(OH)2溶液反应生成NaOH和BaCO3沉淀;
(5)氯化钠溶解度受温度影响较小,硝酸钾溶解度受温度影响较大.
解答 解:(1)Na2CO3固体较稳定,加热条件下不分解,NaHCO3不稳定受热易分解生成Na2CO3,所以可以将固体加热除去碳酸氢钠杂质;
(2)Al易溶于NaOH溶液,但Fe不易溶于NaOH溶液,所以可以用NaOH溶液作除杂剂,然后采用过滤方法得到纯净的Fe;
(3)CuSO4能和Fe反应生成FeSO4,所以用Fe作除杂剂,然后采用过滤方法分离提纯;
(4)Na2CO3能和适量Ba(OH)2溶液反应生成NaOH和BaCO3沉淀,所以可以用适量氢氧化钡溶液作除杂剂,然后采用过滤方法分离提纯;
(5)氯化钠溶解度受温度影响较小,硝酸钾溶解度受温度影响较大,所以可以采用重结晶方法分离提纯,
故答案为:
| 编号 | 物质 | 杂质(少量) | 试 剂 | 除杂操作方法 |
| (1) | Na2CO3固体 | NaHCO3 | - | B |
| (2) | Fe | Al | ① | C |
| (3) | FeSO4 | CuSO4 | ③ | C |
| (4) | NaOH | Na2CO3 | ④ | C |
| (5) | KNO3 | NaCl | - | D |
点评 本题考查物质分离和提纯,为高频考点,把握物质的性质、混合物分离提纯方法等为解答的关键,侧重考查学生分析应用能力,会根据物质性质差异性采用合适的分离提纯方法,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.把1.0mol/L CuSO4溶液、1.0mol/L Fe2(SO4)3溶液两种溶液等体积混合(假设混合后液体的体积等于混合前两种溶液的体积之和),向溶液中加入足量铁粉,经足够长的时间后,铁粉有剩余.此时溶液中Fe2+的物质的量浓度为( )
| A. | 1.0 mol/L | B. | 2.0 mol/L | C. | 3.0 mol/L | D. | 4.0 mol/L |
19.下列说法正确的是( )
| A. | 由H原子形成1 mol H-H键要吸收能量 | |
| B. | 所有燃烧的反应都是放热反应 | |
| C. | NaOH溶于水是放热反应 | |
| D. | 凡经加热而发生的化学反应都是吸热反应 |
16.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 1 mol Na被完全氧化生成Na2O2,失去2NA个电子 | |
| B. | 常温常压下,18 g H2O 中含有的原子总数为3NA | |
| C. | 5.6 g铁粉与硝酸反应失去的电子数一定为0.3NA | |
| D. | 1 mol Cl2与1 mol Fe反应,转移的电子数为3NA |
3.关于Na2CO3和NaHCO3的性质,有关叙述正确的是( )
| A. | 在水中溶解性:Na2CO3>NaHCO3 | |
| B. | 热稳定性:Na2CO3<NaHCO3 | |
| C. | 与酸反应的速度:Na2CO3>NaHCO3 | |
| D. | Na2CO3不能转化成NaHCO3,而NaHCO3能转化为Na2CO3 |
13.下列离子在水溶液中能大量共存的是( )
| A. | H+、K+、HCO3-、Ca2+ | B. | Na+、H+、Cl-、NO3- | ||
| C. | OH-、Na+、Mg2+、HCO3- | D. | Na+、SiO32-、H+、Cl- |
20.下列离子在水溶液中,无色且能大量共存的是( )
| A. | Fe3+、K+、NO3-、Cl- | B. | Na+、K+、Cl-、OH- | ||
| C. | H+、Ba2+、CO32-、SO42- | D. | Na+、K+、OH-、H+ |
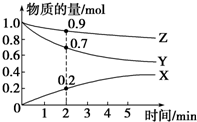 某温度时,在2L容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.由此分析,该反应的化学方程式为3Y+Z?2X;从反应开始至2min时,Z的反应速率为0.025mol•L-1•min-1.
某温度时,在2L容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.由此分析,该反应的化学方程式为3Y+Z?2X;从反应开始至2min时,Z的反应速率为0.025mol•L-1•min-1.
 ,F1和F2互为同分异构体,加成HBr时F1有两种加成产物,F2只有一种加成产物,G1和G2互为同分异构体.请填空:
,F1和F2互为同分异构体,加成HBr时F1有两种加成产物,F2只有一种加成产物,G1和G2互为同分异构体.请填空: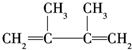 +2NaBr+2H2O;
+2NaBr+2H2O; .
.